时间:2017-08-10 01:17:31
1、填空题 ⑵(12分) 18℃时,H2A(酸):K1=4.3×10-7,K2=2.1×10-12。H2B(酸):K1=1.0×10-7,K2=6.3×10-13,在浓度相同的两种溶液中,用“>”、“<”或“=”填空。
①H+的浓度:H2A________H2B;
②酸根离子的浓度:c (A2-)________c (B2-);
③酸分子的浓度:c (H2A)________c (H2B);
④溶液的导电能力:H2A________H2B。
2、选择题 在体积均为1 L,pH均等于2的盐酸和醋酸中,分别投入0.12 g镁粉充分反应后,下图中比较符合反应事实的曲线是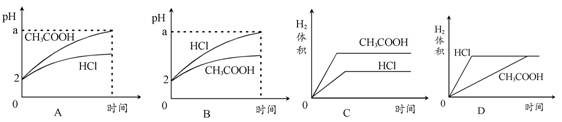
3、选择题 下列各项叙述中不正确的是( )
A.10 ℃ 时NaCl溶解度为35.7g,则此时饱和NaCl 溶液的质量分数小于35.7 %
B.向Na2CO3溶液中加入少量NaHCO3固体,溶液pH 减小
C.50mL 1.0 mol・L-1盐酸与60 mL 1.0 mol・L-1盐酸分别跟50 mL 1.1 mol・L-1NaOH溶液进行反应,中和热数值不相等
D.一定条件下,向水中加入少量NaHSO4,可使水的电离程度减小
4、填空题 炼金废水中含有络离子[Au(CN)2]-,其电离出的CN-有毒,当CN-与H+结合生成HCN时,毒性更强。回答下列问题。
(1)剧毒物HCN的水溶液酸性很弱,写出其电离的方程式:?。
(2)与弱电解质碳酸的电离方式相似,[Au(CN)2]-也存在着两步电离,其一级电离方程式为?。
(3)处理这种废水是在碱性条件下,利用NaClO将CN-氧化为CO32-和N2,其离子方程式为?。在酸性条件下,ClO-也能氧化CN-,但实际处理废水时却不在酸性条件下进行的主要原因是?。
5、填空题 已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度……今有HA、H2B、H3C三种一元、二元、三元弱酸,根据“较强酸 + 较弱酸盐 = 较强酸盐 + 较弱酸”的反应规律,它们之间能发生下列反应:
① HA + HC2-(少量) == A- + H2C-
② H2B(少量) + 2 A- == B2- + 2 HA
③ H2B(少量) + H2C- == HB- + H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C 三种酸中酸性最强的是_____________
(2)A-、B2-、C3-、HB-、H2C-、HC2- 六种离子中,最易结合H+的是______,最难结合H+的是______。
(3)下列反应一定能发生的是_________
A . H3C + 3 A- == 3HA + C3-
B . HB- + A- == HA + B2-
C . H3C + B2- == HB-+ H2C-
(4) 完成下列反应的离子方程式:
① H3C + OH-(过量):______________
② HA(过量) + C3- :_______________