ʱ��:2017-08-08 05:24:01
1��ѡ���� ���б�ʾ���ʽṹ�Ļ�ѧ�����ģ����ȷ����
[? ]
A��8�����ӵ�̼ԭ�ӵĺ��ط��ţ�12C
B��HF�ĵ���ʽ��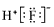
C��Cl-���ӵĽṹʾ��ͼ��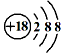
D��CH4���ӵı���ģ�ͣ�
�ο��𰸣�D
���������
�����Ѷȣ���
2��ѡ���� ���к��зǼ��Լ��Ĺ��ۻ�������(? )
A��HCl
B��Na2O2
C��C2H2(����̼ԭ�Ӽ������)
D��CH4
�ο��𰸣�C
���������HCl��ֻ���м��Լ����ǹ��ۻ����Na2O2��Na+����������ӣ�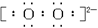 ��֮���γ����Ӽ���
��֮���γ����Ӽ���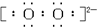 ��Oԭ����Oԭ��֮���γɷǼ��Լ�����Na2O2�����ӻ����C2H2��H��C��C��H����C��H֮���γɼ��Լ���C��C֮���γɷǼ��Լ����ǹ��ۻ����CH4��ֻ���м��Լ����ǹ��ۻ����
��Oԭ����Oԭ��֮���γɷǼ��Լ�����Na2O2�����ӻ����C2H2��H��C��C��H����C��H֮���γɼ��Լ���C��C֮���γɷǼ��Լ����ǹ��ۻ����CH4��ֻ���м��Լ����ǹ��ۻ����
�����Ѷȣ���
3��ѡ���� �����йر���˵���У���ȷ������ǣ�?��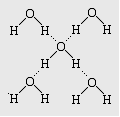
��ˮ���Ӽ����������з��»�����
��ÿ��ˮ���Ӵ��������ĸ�ˮ������Χ�ɵ��������У�
��ÿ��Oԭ�Ӵ����ĸ�Hԭ����Χ�ɵ��������У�
�ܾ�������ʯ���ƣ�?
����ɱ��ľ������ƣ�
��ÿ��ˮ����ƽ��ӵ���ĸ������
�߱��Ľṹ��������ķ����Ժͱ������������ģ�
�����H��Oԭ��֮������������ǦҼ��������
A�����ݢ���
B�����ܢߢ���
C�����ܢݢޢ���
D��ȫ��
�ο��𰸣�A
���������ˮ�����У�ÿ��ˮ����ƽ��ӵ��2�����������ȷ����Ҳ����ģ��������ȷ�ģ���ѡA��
�����Ѷȣ���
4������� ��4�֣�����������Ϥ�����ʣ�
��O2�� ���ʯ �� NaBr �� H2SO4�� Na2CO3�� K2S?��NaHSO4
С��1:��Щ�����У�ֻ�����ۼ�����_______________��ֻ�����Ӽ�����___________���Ⱥ����ۼ��ֺ����Ӽ�����_______________��
С��2:��NaHSO4����ˮ��д������뷽��ʽ______________________________��
�ο��𰸣�
С��1:�٢ڢ�? �ۢ�? �ߢ�?
��2:NaHSO4==Na++H++SO42��
���������(1)���黯ѧ�����жϡ�һ����õĽ����ͻ��õķǽ��������γ����Ӽ����ǽ���Ԫ�ص�ԭ�Ӽ��γɹ��ۼ������Ԣ١����к��еĻ�ѧ���ֱ�Ϊ�Ǽ��Լ����Ǽ��Լ������Ӽ������Լ������Ӽ��ͼ��Լ������Ӽ������Ӽ��ͼ��Լ���
��2�����������ǵ��������ˮ��ȫ���룬���뷽��ʽΪNaHSO4==Na++H++SO42����
�����Ѷȣ�һ��
5������� �밴Ҫ��������и��⣺
��1��MgCl2�ĵ���ʽ��______��������Ľṹ��ʽ��______��
��2��1gC2H2��ȫȼ������CO2��Һ̬ˮ���ų�49.94kJ��������Ȳ����������ȫȼ�յ��Ȼ�ѧ����ʽ��______��
��3����һ�������£�����ʽΪC3H4O2�������ij����Ӧ���ɷ���ʽΪC5H8O2������д���÷�Ӧ�Ļ�ѧ����ʽ���л���д�ṹ��ʽ����ͬ��______��
��4����һ�������£���ϩ�ͱ�ϩ��1��1�����ʵ����ȷ�Ӧ���ɾ��ұ�ϩ�Ļ�ѧ����ʽ��______��
��5����������������ۣ�HCO3-���Կ�����______��
�ο��𰸣���1��þʧȥ2�������γ������ӣ���ԭ�ӵõ������γ������ӣ�����ʽΪ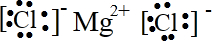 ��������Ľṹ��ʽΪ
��������Ľṹ��ʽΪ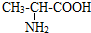 ��
��
�ʴ�Ϊ��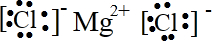 ��
��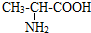 ��
��
��2��1gC2H2��������ȼ������CO2��Һ̬ˮ���ų�49.94kJ������26g��1molCH4��������ȼ������CO2��Һ̬ˮ���ų�1294.8kJ������
���Ȼ�ѧ����ʽΪ��C2H2��g��+52O2��g���T2CO2��g��+H2O��l����H=-1294.8kJ/mol��
�ʴ�Ϊ��C2H2��g��+52O2��g���T2CO2��g��+H2O��l����H=-1294.8kJ/mol��
��3��C3H4O2�������ij����Ӧ���ɷ���ʽΪC5H8O2�������÷�Ӧ�Ļ�ѧ����ʽ��CH2=CHCOOH+CH3CH2OH����
���������
�����Ѷȣ�һ��