时间:2017-08-08 05:08:54
1、选择题 与纯水的电离相似,液氨中也存在着微弱的电离:2NH3 NH4++NH2- 据此判断以下叙述中错误的是
NH4++NH2- 据此判断以下叙述中错误的是
[? ]
A.液氨中含有NH3、NH4+、NH2-等微粒
B.一定温度下液氨中C(NH4+)・C(NH2-)是一个常数
C.液氨的电离达到平衡时C(NH3) = C(NH4+) = C(NH2-)
D.只要不加入其他物质,液氨中C(NH4+) = C(NH2-)
2、选择题 下列有关实验原理、方法和结论都正确都是( )
A.向某FeCl3溶液中加入KSCN溶液,观察到溶液呈血红色,说明该FeCl3溶液中不含Fe2+离子
B.先用水将pH试纸湿润,再测量某未知溶液的pH,若pH=1,说明该溶液中c(H+)=0.1mol?L-1
C.在0.1mol?L-1?Na2CO3溶液中,加两滴酚酞显浅红色,微热后红色加深,说明盐类水解反应是吸热反应
D.等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA>HB
3、选择题 在含有酚酞的0.1mol/L氨水中加少量的NH4Cl晶体,则溶液颜色( )
A.变蓝色
B.变深
C.变浅
D.不变
4、选择题 某一元弱酸HA的溶液中,若未电离的HA分子个数与溶液中的离子个数(忽略水电离)比为a:b,则HA的电离度(即转化率)是
A.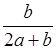 ×100%
×100%
B. ×100%
×100%
C. ×100%
×100%
D.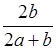 ×100%
×100%
5、选择题 在0.1mol・L-1CH3COOH溶液中存在如下电离平衡: CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
A.加入水时,平衡向生成CH3COOH的方向移动
B.加入少量NaOH固体,平衡向电离的方向移动
C.加入少量0.1mol・L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向电离的方向移动