时间:2017-08-08 04:11:05
1、选择题 下列分子中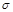 键与
键与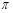 键数之比为3∶1的是(?)
键数之比为3∶1的是(?)
A.N2
B.C2H4
C.HCHO
D.HCN
参考答案:C
本题解析:单键全部是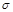 键,双键含有1个
键,双键含有1个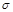 键和1个
键和1个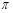 键,三键含有1个
键,三键含有1个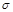 键和2个
键和2个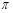 键。所以A~D中
键。所以A~D中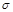 键与
键与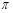 键数之比分别为1︰2、5︰1、3︰1、1︰1,因此正确的答案是C。
键数之比分别为1︰2、5︰1、3︰1、1︰1,因此正确的答案是C。
本题难度:一般
2、填空题 下面的四幅图与所给的四个反应有一一对应关系,请你找出来并填入下面的表格中:
①HCl + NaOH →NaCl + H2O + Q ②H2 + Cl2 2HCl + Q
2HCl + Q
③CaCO3 → CaO + CO2↑ - Q ④Ba(OH)2·8H2O → Ba(OH)2 + 8H2O
参考答案:
本题解析:
本题难度:一般
3、选择题 中和热的测定实验中,可能用到下列仪器:
①托盘天平 ②量筒 ③烧杯 ④温度计 ⑤小试管 ⑥酒精灯。
其中应使用仪器的正确组合是
A.①②⑤
B.②③④
C.②③⑥
D.全部
参考答案:B
本题解析:中和热测定时需要大小不同的两个烧杯、温度计、量筒量取酸碱的体积,故答案选B.
考点:仪器的选用
本题难度:一般
4、选择题 利用储能介质储存太阳能的原理是:白天在太阳光照射下某种固体盐熔化(实为盐溶于自身的结晶水)吸收能量,晚间熔盐释放出相应能量,从而使室温得以调节,已知几种盐的熔点及熔化时能量改变值如表所示:
| 盐 | 熔点/℃ | 质量与相对分子质量相等的盐熔化时吸热/kJ |
| CaCl2·6H2O | 29.0 | 37.3 |
| Na2SO4·10H2O | 32.4 | 77.0 |
| Na2HPO4·2H2O | 36.1 | 100.1 |
| Na2S2O3·5H2O | 48.5 | 49.7 |
参考答案:C
本题解析:由表中所给数据分析:Na2HPO4·12H2O和Na2S2O3·5H2O的熔点高于天气温度,不适合。CaCl2·6H2O和Na2SO4·10H2O比较,后者吸热效果好。
本题难度:一般
5、选择题 有下列两组命题
| A组 | B组 |
| Ⅰ、H—I键键能大于H—Cl键键能 | ①HI比HCl稳定 |
| Ⅱ、H—I键键能小于H—Cl键键能 | ②HCl比HI稳定 |
| Ⅲ、HI分子间作用力大于HCl分子间作用力 | ③HI沸点比HCl高 |
| Ⅳ、HI分子间作用力大于HCl分子间作用力 | ④HI沸点比HCl低 |
参考答案:BC ?
本题解析:可通过比较半径得出键能的大小,半径越小,键长越短,键能越大,分子越稳定;结构相似的分子可比较相对分子质量得出分子间作用力的大小,相对分子质量越大,分子间作用力越大,熔沸点越高(注意某些分子可能有氢键存在)。
本题难度:一般