时间:2017-08-08 04:11:05
1、选择题 DNA分子的两条链之间通过氢键结合。DNA分子复制前首先将双链解开,则DNA分子复制将双链解开的过程可视为(?)
A.化学变化
B.物理变化
C.既有物理变化又有化学变化
D.是一种特殊的生物变化
参考答案:B
本题解析:氢键不是化学键,所以DNA分子复制将双链解开的过程可视为物理变化,答案选B。
点评:该题是基础性试题的考查,难度不大。该题的关键是明确氢键的含义以及物质变化的判断依据,然后结合题意灵活运用即可。
本题难度:简单
2、选择题 对于反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,若有0.1molKMnO4参加反应,下列说法中正确的是
A.还原剂是KMnO4
B.生成Cl25.6L
C.参加反应的HCl为16mol
D.其转移电子为0.5mol
参考答案:D
本题解析:分析:得电子的反应物是氧化剂,失电子的反应物是还原剂,根据元素化合价的变化判断氧化剂和还原剂以及电子转移的数目.
解答:A.该反应中高锰酸钾中的锰元素化合价降低,所以高锰酸钾是氧化剂,故A错误;
B.根据反应方程式知,若有0.1molKMnO4?参加反应,应有0.25mol氯气生成,温度和压强未知,所以无法计算其体积,故B错误;
C.由方程式可知,若有0.1molKMnO4?参加反应,应有0.8molHCl参加反应,故C错误;
D.转移电子的物质的量为0.1mol×(7-2)=0.5mol,故D正确;
故选D.
点评:本题考查氧化还原反应,题目难度中等,易错选项是B,有关气体体积的计算一定要注意温度和压强,没有标明温度和压强,气体摩尔体积不能 用22.4L/mol,为易错点.
本题难度:一般
3、选择题 下列各组物质中,化学键类型相同的是( )
A.HI和NaI
B.NaF和KCl
C.Cl2和NaOH
D.F2和NaBr
参考答案:A、HI中只有共价键,NaI中只有离子键,所以化学键类型不同,故A错误.
B、NaF、KCl中都只有离子键,所以化学键类型相同,故B正确.
C、氯气中只有共价键,氢氧化钠中既有离子键又有共价键,所以化学键类型不同,故C错误.
D、氟气中只有共价键,NaBr中只有离子键,所以化学键类型不同,故D错误.
故选B.
本题解析:
本题难度:简单
4、选择题 下列反应中是吸热反应的是
A.碳酸钙受热分解
B.乙醇燃烧
C.铝粉与氧化铁粉末反应
D.氧化钙溶于水
参考答案:A
本题解析:A.碳酸钙在高温下的分解反应是吸热反应,故A正确;
B.乙醇燃烧是氧化反应,是常见放热反应,故B错误;
C.铝粉与氧化铁粉末反应,是放热反应,故C错误;
D.氧化钙与水反应放出大量的热,则属于放热反应,故D错误。
故选A。
考点:吸热反应和放热反应
点评:本题考查吸热反应,难度不大,掌握中学化学中常见的吸热或放热的反应是解题的关键。
本题难度:一般
5、填空题 通常人们把拆开1mol?某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。?
化学键?Si―O?Si―Cl?H―H?H―Cl?Si―Si?Si―C?
键能/?kJ?mol―1?460?360?436?431?176?347?
请回答下列问题:?
⑴?比较下列两组物质的熔点高低(填>或<)?
SiC______?Si;?SiCl4?______?SiO2?
⑵?图立方体中心的“●”表示硅晶体中的一个原子,?请在立方体的顶点用“●”表示出与之紧邻的硅原子。?
⑶?工业上高纯硅可通过下列反应制取:?SiCl4?(g)?+?2H2(g)?Si(s)?+?4HCl(g);该反应的反应热△H?=?___________?KJ/mol
参考答案:(1)>?<?
(2)如下图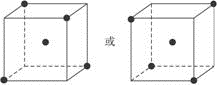
本题解析:本题主要考查键能的大小与物质性质及反应热之间的关系。
(1)SiC与Si皆为原子晶体,由于Si―C的键能大于Si―Si的键能,故SiC的熔点比Si高;SiCl4为分子晶体,SiO2为原子晶体,前者的熔点低于后者。
(2)根据硅原子与硅原子可形成4个相等的硅硅键可知除立方体中心的硅原子处,与它相邻的硅原子应处于可形成正四面体的4个顶点上。
本题难度:一般