时间:2017-08-06 11:03:28
1、选择题 室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中c(CH3COO-)/[c(CH3COOH)・・c(OH-)]不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
参考答案:B
本题解析:加水稀释,平衡向正向移动,导电粒子的数目增大,其浓度减少了,A错;温度不变,B项中表达式中上下同乘以c(H+),则表达式变为Ka/Kw,B正确;醋酸的电离程度越大,c(H+)不一定增大,比如加水稀释,C错;从表面上看,加入氢氧化钠溶液,刚好中和,其实醋酸是弱酸,部分电离与氢氧化钠“刚好中和”,醋酸的起始浓度远大于它电离出的c(H+),故醋酸过量,中和后显酸性,D错。答案选B。
本题难度:一般
2、选择题 常温下,0.1 mol/L某一元酸(HA)溶液中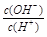 =1×10-8,下列叙述正确的是(? )
=1×10-8,下列叙述正确的是(? )
A.溶液中水电离出的c(H+)=10-10 mol/L?
B.溶液中c(H+)+c(A-)=0.1 mol/L
C.溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
D.与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为c(A-)>c(Na+)>c(OH-)>c(H+)
参考答案:C
本题解析:0.1 mol/L某一元酸(HA)溶液中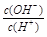 =1×10-8,而溶液中c(H+)・c(OH-)=10-14.解得c(OH-)=10-11.所以c(H+)10-3mol/L<c(HA),所以该酸是弱酸。A.所以溶液中水电离出的c(H+)=c(OH-)=10-11 mol/L。错误。B.根据物料守恒可得c(HA)+c(A-)=0.1 mol/L。错误。C.在弱酸的溶液中存在电离平衡HA
=1×10-8,而溶液中c(H+)・c(OH-)=10-14.解得c(OH-)=10-11.所以c(H+)10-3mol/L<c(HA),所以该酸是弱酸。A.所以溶液中水电离出的c(H+)=c(OH-)=10-11 mol/L。错误。B.根据物料守恒可得c(HA)+c(A-)=0.1 mol/L。错误。C.在弱酸的溶液中存在电离平衡HA A-+H+。溶液中加入一定量CH3COONa晶体,由于会发生反应CH3COO-+ H+=CH3COOH,会使c(H+)减小,所以根据水的离子积常数不变可知溶液的c(OH-)增大;若加水稀释,由于离子浓度减小的倍数多,所以平衡向电离的方向移动。由于稀释的倍数大于平衡移动增大的倍数。所以c(H+)减小。正确。D.若与0.05mol/LNaOH溶液等体积混合后,则得到的溶液为NaA与HA等浓度、等体积的混合溶液。由于酸的电离大于盐的水解,所以c(A-)>c(Na+)>c(H+)>c(OH-)。错误。
A-+H+。溶液中加入一定量CH3COONa晶体,由于会发生反应CH3COO-+ H+=CH3COOH,会使c(H+)减小,所以根据水的离子积常数不变可知溶液的c(OH-)增大;若加水稀释,由于离子浓度减小的倍数多,所以平衡向电离的方向移动。由于稀释的倍数大于平衡移动增大的倍数。所以c(H+)减小。正确。D.若与0.05mol/LNaOH溶液等体积混合后,则得到的溶液为NaA与HA等浓度、等体积的混合溶液。由于酸的电离大于盐的水解,所以c(A-)>c(Na+)>c(H+)>c(OH-)。错误。
本题难度:一般
3、选择题 用pH均为2的盐酸和醋酸溶液,分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗盐酸和醋酸溶液的体积分别为Vl和V2,则Vl和V2的关系正确的是
[? ]
参考答案:A
本题解析:
本题难度:一般
4、选择题 电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。下图是用KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线示意图。 下列示意图中,能正确表示用NH3・H2O溶液滴定HCl和CH3COOH混合溶液的滴定曲线的是
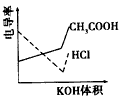
[? ]
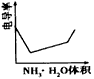
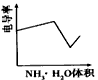
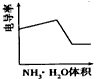
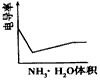
参考答案:D
本题解析:
本题难度:一般
5、选择题 根据下表数据,比较在相同温度下下列三种酸的相对强弱,正确的是 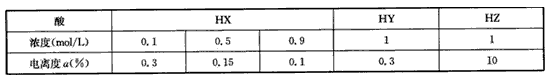
[? ]
A.HX>HY>HZ
B.HZ>HX>HY
C.HY>HZ>HX
D.HZ>HY>HX
参考答案:D
本题解析:
本题难度:一般