时间:2017-08-06 09:23:27
1、选择题 常温下,将浓度均为0.1mol/L一元酸HA溶液和NaOH溶液等体积混合,得到混合溶液①,该混合溶液pH=9,下列说法正确的是
A.①溶液中:c(A¯)>c(Na+)>c(OH¯)>c(H+)
B.①溶液中:c(HA)+c(A¯)=0.1mol/L
C.常温下,0.1mol/LHA溶液的pH=1
D.0.1mol/LHA溶液中:c(HA)>c(A¯)
2、选择题 已知同温度下,三种酸的电离平衡常数的大小关系为Ka(HX)>Ka(HY)>Ka(HZ),则物质的量浓度相同的三种盐NaX、NaY和NaZ溶液pH由大到小的顺序是
A.NaX NaY NaZ
B.NaX NaZ NaY
C.NaY NaZ NaX
D.NaZ NaY NaX
3、填空题 根据所学知识完成下列空白。
Ⅰ.(1)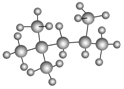 的名称(系统命名法)是 。
的名称(系统命名法)是 。
(2)(CH3)3CCH2CH(CH2CH3)CH(CH3)2的名称(系统命名法)是 。
(3)2,3-二甲基-4-乙基已烷 的结构简式______________________________。
Ⅱ.某盐的化学式为XmYn(m≠n),在水中能完全电离:XmYn=mXn++nYm-。将一定量的盐溶于足量水时:
(1)若测得溶液的pH为9,则该盐与水反应的离子方程式可能为: (用X或Y表示)。
(2)若X、Y为同周期的短周期元素,XmYn溶于水时,有白色沉淀产生,又有无色气体放出,则XmYn溶于水的化学方程式为:_________________________(用元素符号表示)。
4、填空题 酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下:
回答下列问题:
(1)SnCl2用盐酸而不用水直接溶解的原因是
加入锡粉的作用是
(2)反应I生成的沉淀为SnO,写出该反应的化学方程式:
(3)检验沉淀已经“洗涤”干净的操作是: (3分)
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH。若溶液中c(Sn2+)=1.0mol・L―1,则室温下应控制溶液pH 。(已知:Ksp[Sn(OH)2]=1.0×10―26)
(5)酸性条件下,SnSO4还可用作双氧水的去除剂,试写出所发生反应的离子方程式:
。
(6)潮湿环境中,镀锡铜即使锡层破损也能防止形成铜绿,请结合有关的原理解释其原因:
。
5、选择题 25℃时,向10mL0.01mol・L-1KOH溶液中滴加0.01mol・L-1苯酚溶液,混合溶液中粒子浓度关系正确的是
A.当pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-)
B.当pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-)
C.V[C6H5OH(aq)]=10mL时,c(K+)=c(C6H5O-)>c(OH-)=c(H+)
D.V[C6H5OH(aq)]=20mL时,c(C6H5O-)+c(C6H5OH)=2c(K+)