时间:2017-08-01 01:00:00
1、选择题 某溶液中在25℃时由水电离出的氢离子浓度为1×10-12 mol/L,下列说法正确 的是(?)
的是(?)
A.HCO3-离子在该溶液中一定不能大量共存
B.该溶液的pH一定是12
C.向该溶液中加入铝片后,一定能生成氢气
D.若该溶液的溶质只有一种,它一定是酸或碱
参考答案:A
本题解析:略
本题难度:一般
2、实验题 (12分)如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题: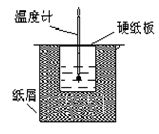
(1)从实验装置上看,图中伤缺少的一种玻璃仪器是_____________;
(2)烧杯间填满碎纸条的作用是____________________;
(3)若大烧杯上不盖硬纸板,求得的反应热数值__________(填“偏大”“偏小”或“无影响”)。
(4)实验中该用60 mL 0.50 mol·L-1HCl跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会________(填“偏大”“偏小”或“无影响”)。
参考答案:(12分)(1)环形玻璃搅拌棒? (2)减少实验过程中的热量损失
(3)偏小? (4)不相等;相等;(5)偏小
本题解析:(1)在实验过程中,需要搅拌,所以还缺少环形玻璃搅拌棒。
(2)由于在实验过程中,需要尽可能的减少热量的损失,因此烧杯间填满碎纸条的作用是减少实验过程中的热量损失。
(3)若大烧杯上不盖硬纸板,则会导致热量的损失,因此求得的反应热数值偏小。
(4)改变酸或碱的用量,可以改变反应中放出的热量,但不能改变中和热,因为中和热是在一定条件下,稀溶液中酸和碱反应生成1mol水时放出的热量,因此中和热时不变的。
(5)由于氨水中存在电离平衡,而电离是吸热的,所以测得的中和热数值会减小。
本题难度:一般
3、选择题 下列叙述正确的是(?)
A.HCl和NaOH反应的中和热为ΔH=–57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为ΔH=2×(–57.3)kJ/mol
B.CO(g)燃烧热ΔH=–283.0kJ/mol,则2CO2(g) =" 2CO(g)" + O2(g)反应的ΔH=+2×283.0kJ/mol
C.用等体积的0.50mol·L-1盐酸、0.55mol·L-1NaOH溶液进行中和热测定的实验,会使测得的值偏大
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
参考答案:B
本题解析:中和热一定的,ΔH=–57.3kJ/mol。测定时碱稍稍过量为了反应完全,1mol甲烷燃烧生成液态水和二氧化碳所放出的热量是甲烷的燃烧热。
本题难度:一般
4、选择题 现有1 L?0.5mol/L的硫酸钠溶液,有关溶液的叙述正确的是( ?)。
A.取0.5 L溶液,Na+的浓度是0.5 mol/L
B.取0.1 L溶液稀释至l L,SO42-离子浓度是0.05 mol/L
C.溶质的离子总数是6.02 x 1023个
D.该溶液是把0.5 mol Na2SO4溶于1 L水中配制而成的
参考答案:B
本题解析:0.5mol/L的硫酸钠溶液中钠离子的浓度是0.5mol/L×2=1mol/L。又因为溶液是均一稳定的,所以A中钠离子的浓度仍然是1mol/L,A错误;0.1 L溶液稀释至l L,SO42-离子浓度变为0.5mol/L÷10=0.05mol/L,所以选项B正确;硫酸钠的物质的量是0.5mol,离子的总物质的量是1.5mol,C不正确;D不正确,因为溶液的体积不是1L,答案选B。
点评:该题是中等难度的试题,试题基础性强,侧重能力的考查和解题方法的指导。有助于培养吸收的逻辑思维能力和灵活应变能力,提高学生分析问题、解决问题的能力。
本题难度:简单
5、选择题 已知反应:① 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
② 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol 下列结论正确的是
[? ]
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量
参考答案:AC
本题解析:
本题难度:简单