时间:2017-07-27 11:12:06
1、选择题 下列各组物质的燃烧热相等的是
[? ]
A.碳和一氧化碳
B.1mol碳和2mol碳
C.1mol乙炔和2mol碳
D.淀粉和纤维素
参考答案:B
本题解析:
本题难度:简单
2、填空题 按要求回答下列问题
(1)某温度下,纯水中c (H+)=2.0×10-7 mol・L-1,则此时c (OH-) =?mol・L-1
0.9mol・L-1NaOH溶液与0.1mol・L-1HCl溶液等体积混合(不考虑溶液体积变化)后,溶液的pH=_____。
(2)向0.020 mol・L-1的HCN溶液中加入0.020 mol NaCN固体,溶液pH增大,主要原因是?;已知该混合溶液中c (Na+) > c (CN-),则c (HCN)?c (CN-)(用“>”、“<”、“=”符号填空)。
(3)向1L 0.10 mol・L-1的HCN溶液中加入0.08molNaOH固体,得到混合溶液,则_________和__________两种粒子的物质的量之和等于0.1mol;写出该混合溶液中存在的所有平衡的表达式?。
参考答案:(1)2.0×10-7 (2分) ;13 (2分)
(2)CN-浓度增大,抑制了HCN的电离,使C(H+)降低,pH值增大,>(2分)
(3)HCN、 CN-(2分,少答一个不得分);
H来源:91考试网 91EXAm.orgCN  ?H++ CN-(1分);H2O
?H++ CN-(1分);H2O  ?H+ + OH-(1分);CN-+ H2O
?H+ + OH-(1分);CN-+ H2O HCN+ OH- (1分);
HCN+ OH- (1分);
本题解析:(1)纯水呈中性,即c (H+)="c" (OH-) =2.0×10-7 mol・L-1,Kw=4.0×10-14,0.9mol・L-1NaOH溶液与0.1mol・L-1HCl溶液等体积混合,
c (OH-) =(0.9-0.1)/2=0.4mol/L,故c (H+)="Kw/c" (OH-)=4.0×10-14/0.4mol/L=10-13mol/L,所以pH="-lgc" (H+)=13;(2)向0.020 mol・L-1的HCN溶液中加入0.020 mol NaCN固体,溶液pH增大,主要原因为CN-浓度增大,抑制了HCN的电离,使C(H+)降低,pH值增大,因为c (Na+) > c (CN-),根据电荷守恒c (H+)+c (Na+)="c" (CN-)+c (OH-),,即该溶液层碱性,所以HCN的电离小于水解,即c (HCN)>c (CN-);(3)根据物料守恒,可以知道)HCN、 CN两种粒子的物质的量之和等于0.1mol;该溶液为NaCN和HCN的混合溶液,所以混合溶液中存在的所有平衡的表达式为CN  ?H++ CN-;H2O
?H++ CN-;H2O  ?H+ + OH-;CN-+ H2O
?H+ + OH-;CN-+ H2O HCN+ OH- 。
HCN+ OH- 。
点评:本题综合考查了水的离子积、盐类水解、电荷守恒、质子守恒、pH的计算,有一定的综合性,该题有一定的难度。
本题难度:一般
3、选择题 下列热化学方程式中△H代表燃烧热的是
A.CH4 ( g ) + 3/2O2 ( g ) = 2H2O ( l ) + CO ( g )△H1
B.S ( s ) + 3/2O2 ( g ) = SO3 ( s )△H2
C.C6H12O6 ( s ) + 6O2 ( g ) = 6CO2 (g) + 6H2O ( l )△H3
D.CO ( g ) +1/2 O2 ( g ) = CO2 ( g )△H4
参考答案:CD
本题解析:A 错误,应该生成二氧化碳
B 错误,应该生成二氧化硫
C 正确,碳、氢两元素都生成了稳定的氧化物。
D 正确,碳元素生成了稳定的氧化物二氧化碳。
本题难度:一般
4、填空题 已知某溶液中只存在OH-、H+、NH、Cl-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH)>c(H+)>c(OH-)? ②c(NH)>c(OH-)>c(Cl-)>c(H+)
③c(NH)>c(Cl-)>c(OH-)>c(H+)? ④c(Cl-)>c(H+)>c(NH)>c(OH-)
填写下列空白
(1)若溶液中只溶解一种溶质,则该溶质是________,上述四种离子浓度的大小顺序为(填序号)________;
(2)若四种离子的关系符合④,则溶质为________;
(3)则pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数,下列图像正确的是(填图像符号)________;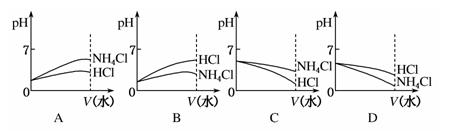
(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3・H2O)(填“大于”“小于”或“等于”)
参考答案:(1) NH4Cl ①?(2)HCl? NH4Cl?(3)B?(4) 小于
本题解析:略
本题难度:简单
5、填空题 (8分)在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
(1)该温度下,水的离子积常数kw=?。
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=?。
(3)该温度下,若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,a和b之间应满足的关系是?。(列出含a、b的式子)
(4)该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因?。
参考答案: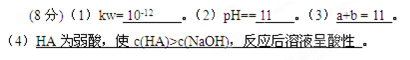
本题解析:(1)该温度下,水的离子积常数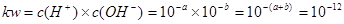 ;
;
(2)100mL0.1mol/L的稀硫酸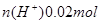 ;100mL0.4mol/L的NaOH溶液
;100mL0.4mol/L的NaOH溶液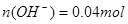 ;混合后,溶液中氢氧根离子过量,剩余物质的量为:
;混合后,溶液中氢氧根离子过量,剩余物质的量为: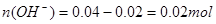 ;则
;则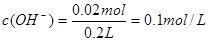 ,即
,即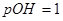 ,
,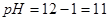 ;
;
(3)混合后溶液呈中性即酸与碱恰好完全反应,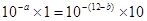 ,得
,得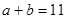 ;
;
(4)pH=2的某酸HA溶液和pH=10的NaOH溶液中氢离子浓度与氢氧根离子浓度相等,等体积混合溶液显酸性,即可得HA为弱酸;
本题难度:一般