时间:2017-07-27 10:37:36
1、填空题 (14分)下列物质中:①NaCl ②Na2O ③CH3COOH ④CO2 ⑤NaHCO3 ⑥NH3·H2O ⑦HCl ⑧NaOH ⑨Cl2 ⑩酒精 请按要求回答下列问题(填编号):
(1) 属于电解质的有 ? ;(2)属于非电解质的有: ? ? ;
(3)属于强电解质的有?;(4)属于弱电解质的有?;
(5)请分别写出NH3·H2O ,NaHCO3的电离方程式:?;???。
参考答案:(共14分)
(1) ①②③⑤⑥⑦⑧?(2)④⑩?(3)①②⑤⑦⑧?(4)③⑥? (各2分)
(5)NH3·H2O 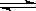 ?NH4 ++OH-;NaHCO3=Na ++ HCO3-(各3分)
?NH4 ++OH-;NaHCO3=Na ++ HCO3-(各3分)
本题解析:(1) 属于电解质的有 ①②③⑤⑥⑦⑧ ;(2)属于非电解质的有:④⑩;
(3)属于强电解质的有①②⑤⑦⑧;(4)属于弱电解质的有③⑥;
(5)NH3·H2O的电离方程式:NH3·H2O 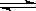 ?NH4 ++OH-;?
?NH4 ++OH-;?
NaHCO3的电离方程式?NaHCO3=Na ++ HCO3-。
点评:水溶液中或熔融状态下能够电离的化合物称为电解质,常见的酸、碱、盐都是电解质如:碳酸、硫酸、硝酸、磷酸、乙酸(醋酸)都是酸,氢氧化钡、一水合氨、氢氧化铜都是碱,碳酸钠、碳酸钙、碳酸氢钠、硫酸铜晶体都是盐,它们都是电解质。在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质。(大多数的有机物都是非电解质)(单质,混合物不管在水溶液中或熔融状态下是否[1]能够导电,都不是电解质或非电解质。)
在水溶液中几乎完全发生电离的电解质叫做强电解质;在水溶液中不完全发生电离的电解质叫做弱电解质。
电解质与非电解质的区别
?
电解质
非电解质
相同点
均为化合物
不同点
水溶液或熔融状态能导电
水溶液和熔融状态都不能导电
本质区别
在水溶液里或熔融状态下自身能发生电离
在水溶液里或熔融状态下自身不能发生电离
所含物质类型
酸, 碱, 盐 , 活泼金属氧化物,水
非金属氧化物,非酸性气态化合物,部分有机物
电解质是指在水溶液中或熔融状态下能够导电的化合物,例如酸、碱和盐等。凡在上述情况下不能导电的化合物叫非电解质,例如蔗糖、酒精等。
能导电的化合物不一定是电解质,判断某化合物是否是电解质,不能只凭它在水溶液中导电与否,还需要进一步考察其晶体结构和化学键的性质等因素。例如,判断硫酸钡、碳酸钙和氢氧化铁是否为电解质。硫酸钡难溶于水,溶液中离子浓度很小,其水溶液不导电,似乎为非电解质。但熔融的硫酸钡却可以导电。因此,硫酸钡是电解质。碳酸钙和硫酸钡具有相类似的情况,也是电解质。从结构看,对其他难溶盐,只要是离子型化合物或强极性共价型化合物,尽管难溶,但溶的那部分是完全电离的,所以也是电解质。因为溶解是绝对的,不溶是相对的。没有绝对不溶的物质。
本题难度:一般
2、选择题 25℃时,将氨水与氯化铵溶液混合得到 c(NH3·H2O)+c(NH4+) = 0.1mol·L-1的混合溶液。溶液中c(NH3·H2O)、c(NH4+)与pH的关系如图所示。下列有关离子浓度关系叙述一定正确的是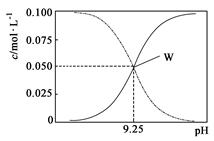
A.W点表示溶液中:c(NH4+) +c(H+) = c(Cl-)+c(OH-)
B.pH=10.5溶液中:c(Cl-)+c(OH-)+c(NH3·H2O)<0.1mol·L-1
C.pH=9.5溶液中:c(NH3·H2O)>c(NH4+)>c(OH-)>c(H+)
D.向W点所表示1L溶液中加入0.05molNaOH固体(忽略溶液体积变化):c(Cl-)>c(Na+)>c(OH-) >c(NH4+) >c(H+)
参考答案:AC
本题解析:A、根据电荷守恒知,二者的混合液中一定有:c(NH4+) +c(H+) = c(Cl-)+c(OH-),正确;B、根据电荷守恒知,二者的混合液中一定有:c(NH4+) +c(H+) = c(Cl-)+c(OH-),又c(NH3·H2O)+c(NH4+) = 0.1mol·L-1,则pH=10.5溶液中:c(Cl-)+c(OH-)+c(NH3·H2O)>0.1mol·L-1,错误;C、根据题给图像知pH=9.25的混合液中c(NH3·H2O)=c(NH4+),pH=9.5溶液中:c(NH3·H2O)>c(NH4+)>c(OH-)>c(H+),正确;D、向W点所表示1L溶液中加入0.05molNaOH固体所得溶液为氯化钠与一水合氨的混合液,则有:c(Cl-)=c(Na+)>c(OH-) >c(NH4+) >c(H+),错误。
考点:考查离子浓度大小比较,三个守恒式得应用。
本题难度:困难
3、选择题 醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是(?)
H++CH3COO-,下列叙述不正确的是(?)
A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小
C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D.常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
参考答案:B
本题解析:A.在醋酸溶液中存在的阳离子是H+、阴离子是OH-和CH3COO-。根据电荷守恒可知,醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)。正确。B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(H+)减小。由于在溶液中存在Kw=c(H+)·c(OH-).所以c(OH-)增大。错误。C. 醋酸溶液中存在电离平衡CH3COOH H++CH3COO-加少量的CH3COONa固体,c(CH3COO-)增大。根据平衡移动原理,增大生成物的浓度,平衡向逆向移动。正确。D.由于CH3COOH是弱酸,部分电离,而NaOH是强碱,完全电离。在常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液电离产生的c(H+)=c(OH-)=10—2mol/L.等体积混合后,电离的H+恰好完全被中和,这时破坏了醋酸的电离平衡,醋酸会继续电离产生H+和CH3COO-直至达到新的平衡,由于此时溶液的c(H+)>c(OH-),所以pH<7。正确。
H++CH3COO-加少量的CH3COONa固体,c(CH3COO-)增大。根据平衡移动原理,增大生成物的浓度,平衡向逆向移动。正确。D.由于CH3COOH是弱酸,部分电离,而NaOH是强碱,完全电离。在常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液电离产生的c(H+)=c(OH-)=10—2mol/L.等体积混合后,电离的H+恰好完全被中和,这时破坏了醋酸的电离平衡,醋酸会继续电离产生H+和CH3COO-直至达到新的平衡,由于此时溶液的c(H+)>c(OH-),所以pH<7。正确。
本题难度:一般
4、选择题 部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | K1=1.77×10-4 | K1=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
参考答案:C
本题解析:A. HCOOH和HCN都是弱酸,由于HCOOH的电离平衡常数大于HCN,所以等体积、等pH的HCOOH和HCN溶液中溶质的物质的量n(HCN)>n(HCOOH),所以反应消耗的NaOH的量n(HCN) >n(HCOOH),正确;B.由于酸性HCOOH>HCN,根据盐的水解规律:谁弱显谁性,越弱越水解,所以相同温度时,等浓度的HCOONa和NaCN溶液的pH前者小于后者,正确;C.由于HCN 的电离平衡常数小于H2CO3的一极电离平衡常数,大于碳酸的二级电离平衡常数,所以发生反应:CN-+H2O+CO2 = HCN+HCO3-,错误;D.由于甲酸的电离平衡常数大于碳酸的一极电离平衡常数,所以发生反应:2HCOOH+CO32-= 2HCOO-+H2O+CO2↑,正确。
考点:考查弱酸的电离平衡常数在反应的进行、酸碱中和、盐的水解中的应用的知识。
本题难度:一般
5、填空题 (10分) 25℃时,电离平衡常数:
| 化学式 | CH3COOH | H2CO3 | HClO | H2C4H4O6(酒石酸) | H2SO3 |
| 电离平衡常数 | 2.0×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 | K1=9.1×10-4 K2=4.3×10-5 | K1=1.3×10-2 K2=6.3×10-8 |
参考答案:(1) e c d b a (2)2.85(2分)(3)BC E
(4) CO2+ NaClO+ H2O= NaHCO3+ HClO
(5)(0.05+10-6-10-8)mol/L 或0.05000099 mol/L
本题解析:(1)分析题给电离平衡常数知,酸性:HC4H4O6—>CH3COOH> H2CO3>HClO> HCO3—,根据盐类水解规律:形成盐的酸根对应酸越弱,该盐的水解程度越大,同浓度溶液的碱性越强,PH越大,可知,物质的量浓度相同这五种盐溶液的PH:Na2CO3>NaClO >NaHCO3>CH3COONa> Na2C4H4O6,则pH相同的五种盐溶液的物质的量浓度:Na2CO3<NaClO <NaHCO3<CH3COONa< Na2C4H4O6,由大到小的顺序是e c d b a;(2)设0.1mol/L的CH3COOH溶液中氢离子浓度为x,代入醋酸的电离常数表达式得:x2/0.1=2.0×10-5,解得x=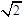 ×10-3,PH=2.85;(3)根据题给信息知,将0.1mol/L的次氯酸溶液与0.1mol/L的碳酸钠溶液等体积混合,发生的反应为:
×10-3,PH=2.85;(3)根据题给信息知,将0.1mol/L的次氯酸溶液与0.1mol/L的碳酸钠溶液等体积混合,发生的反应为:
HClO+ Na2CO3= NaClO+ NaHCO3,所得溶液为浓度均为0.05mol/L的NaClO和 NaHCO3的混合液,A、ClO-的水解程度大于HCO3-,则c(HCO3-) >c(ClO-) ,错误;B、c(Na+) > c(HCO3-) >c(ClO-) > c(H+),正确;C、根据物料守恒知,c(Na+)="c(HClO)" +c(ClO-)+ c(HCO3-) + c(H2CO3)+ c(CO32-),正确;D、根据电荷守恒知,c(Na+) + c(H+)= c(ClO-)+ c(HCO3-) + 2c(CO32-)+ c(OH-),错误;E、根据物料守恒和电荷守恒知,c(HClO) + c(H+)+ c(H2CO3)= c(OH-) + c(CO32-),正确;选BCE;(4)根据题意知H2CO3>HClO> HCO3—,少量的CO2通入NaClO溶液中的化学方程式为CO2+ NaClO+ H2O= NaHCO3+ HClO;(5)0.1mol/L的酒石酸溶液与pH=13的NaOH溶液等体积混合,所得溶液为0.05mol/L的NaHC4H4O6,根据电荷守恒式可知,c(HC4H4O6-)+2 c(C4H4O62-)= c(Na+) + c(H+) —c(OH-)= (0.05+10-6-10-8)mol/L ="0.05000099" mol/L。
考点:考查电解质溶液,涉及弱电解质的电离和盐类的水解。
本题难度:困难