时间:2017-07-27 10:02:07
1、填空题  某化学兴趣小组模拟工业上从铝土矿(主要成分是
某化学兴趣小组模拟工业上从铝土矿(主要成分是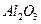 ,含
,含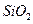 、
、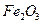 等杂质)中提取氧化铝的工艺做实验,流程如下:
等杂质)中提取氧化铝的工艺做实验,流程如下: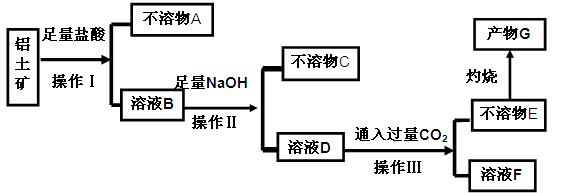

 请回答下列问题:
请回答下列问题: (1)操作Ⅰ、Ⅱ、Ⅲ的名称为 。
(1)操作Ⅰ、Ⅱ、Ⅲ的名称为 。 (2)不溶物C是 (填化学式),不溶物E是 (填化学式),写出B→D反应的离子方程式 。
(2)不溶物C是 (填化学式),不溶物E是 (填化学式),写出B→D反应的离子方程式 。 (3)溶液F中含碳元素溶质的主要成份是 (填化学式),说出它的一种用途 。
(3)溶液F中含碳元素溶质的主要成份是 (填化学式),说出它的一种用途 。
参考答案:(1)过滤(1分)
(2)Fe(OH)3 (2分)?Al(OH)3?(2分)
Al3++4O H-=AlO2-+2H2O(2分)
H-=AlO2-+2H2O(2分)
(3)NaHCO3(2分)?发酵粉、食品膨松剂、治胃酸过多、制纯碱等(1分)
本题解析:略
本题难度:简单
2、选择题 物质的量为0.20 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为
A.6.4g
B.8.0g
C.8.4g
D.9.2g
参考答案:D
本题解析:若气体只有CO2,有2Mg+CO==2MgO+C可知,0.20 molMg生成0.20 molMgO和0.10molC,共计9.2g,因含有O2而低于此计量,但多余Mg自身质量4.8g。故选D。
本题难度:一般
3、填空题 用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)Al的原子结构示意图为____________;Al与NaOH溶液反应的离子方程式为____________。
(2)30Si的原子的中子数为________________________。
(3)Al3+与Yn-的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是____________________________________。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是____________。
(5)经处理后的熔渣36.0 g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0 g固体;滤液中加入过量NaOH溶液,分离得到21.4 g固体;则此熔渣中Al2O3的质量分数为____________。
参考答案:(1) ? 2Al+2OH-+2H2O=
? 2Al+2OH-+2H2O=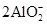 +3H2↑
+3H2↑
(2)16
(3)HCl
(4)CO2
(5)25%
本题解析:(3)根据Y所在族各元素的氢化物的水溶液均显酸性,可推知Y为F,回答沸点时要考虑到HF中含有氢键。
(5)在熔渣中加入盐酸,发生的反应为:Fe2O3+6HCl=2FeCl3+3H2O,Al2O3+6HCl=2AlCl3+3H2O,11.0 g为SiO2的质量。
在滤液中加入过量NaOH溶液,发生的反应为:
FeCl3+3NaOH=Fe(OH)3↓+3NaCl
AlCl3+4NaOH=NaAlO2+3NaCl+2H2O,所得21.4 g固体为Fe(OH)3,根据关系式:
2Fe(OH)3~Fe2O3
214? 160
21.4 g? m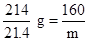 ? m="16" g
? m="16" g
由此可知:
Al2O3的质量="36.0" g-11.0 g-16.0 g="9.0" g,
故Al2O3的质量分数=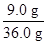 ×100%=25%。
×100%=25%。
本题难度:一般
4、选择题 能用铝槽车运输的是
A.浓硫酸
B.稀硝酸
C.浓盐酸
D.氢氧化钠溶液
参考答案:A
本题解析:应该选A,因为铝与浓硫酸发生钝化,阻止反应的进一步进行,所以可以用来运输。
BCD都会与铝发生氧化还原反应,使铝槽车发生腐蚀,所以不能用铝槽车来运输它们。
本题难度:简单
5、填空题 锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式__________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是___________。
①硫酸铝和氢氧化钠②硫酸铝和氨水③硫酸锌和氢氧化钠④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式________________________。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因____________________________。
参考答案:(1)AlO2-或Al(OH)4-
(2)Zn+2NaOH = Na2ZnO2+H2↑ 或Zn+2NaOH+2H2O = Na2Zn(OH)4+ H2↑
(3)①③④
(4)Al3++3NH3·H2O = Al(OH)3↓ +3NH4+ ;可溶性锌盐与氨水反应产生的Zn(OH)2可溶于过量氨水中,生成Zn(NH3)42+,氨水的用量不易控制
本题解析:
本题难度:一般