ʱ��:2017-07-27 09:25:08
1���ƶ��� X��Y��Z���ֶ�����Ԫ�أ�����֮�������5�ֻ�����A��B��C��D��E��X��Y��Z����Ԫ�ؿ���ɻ�����F����֪��������A��B��C��ԭ�Ӹ����ȶ�Ϊ1�U1��BΪ����ɫ���壬C��E�����¾�Ϊ��ɫҺ�壻A�ǻ�ѧʽΪXZ�����ӻ����A��E��Ӧ����F��һ�����壻D�ǻ�ѧʽΪX2Y�����ӻ����D�����������Ӿ�����ͬ�ĵ��Ӳ�ṹ����E����������������ȡ� ��ش��������⣺
��1��XԪ�ص�������________________
��2��X��Y��Z��ԭ�Ӱ뾶�Ӵ�С��˳���ǣ���Ԫ�ط��ű�ʾ��____________________
��3��д��F�ĵ���ʽ______________________________
��4����֪X���ʡ�A��B��D���壬�ֱ���E��Ӧ������ͬһ�����ʣ�����X���ʡ�A��B�ֱ���E�ķ�Ӧ����������ԭ��Ӧ����д��X���ʡ�B�ֱ���E��Ӧ�Ļ�ѧ����ʽ____________________________��
?___________________________��B�к��еĻ�ѧ����___________�����һ��˵��B����;______________________________
��5����д���ɻ�����C��ȡY�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽ_______________________________
2��ѡ���� �ɶ����ڵ�����Ԫ����ɵĻ�����XY3������˵���������
[? ]
3���ƶ��� X��Y��ZΪ���ֶ�����Ԫ�أ��˵��������������X��Y��Z����Ԫ�ص�ԭ�Ӻ�����Ӳ���֮��Ϊ5����֪X��ԭ�ӽṹ���Ԫ�أ�YԪ��ԭ��������Ӳ��ϵĵ����������������2����ZԪ����ֲ����������ҪӪ��Ԫ�ء���ش��������⣺
��1���ƶ�X��Y��Z��Ԫ�أ�X________��Y_________��Z__________��дԪ�ط��ţ���
��2��YԪ�صĵ�������һ�ֳ�Ϊ����ϡ�ķ���Y?���������������ķ�Ӧ��______�� ?A����ȥ��Ӧ?B��ȡ����Ӧ?C���ӳɷ�Ӧ?D���ۺϷ�Ӧ
��3��Z��X���γɶ��ֻ��������ZX?�ĵ���ʽΪ________________�������ƶϳ���X��Z��Ԫ�ط��ű�ʾ��
��4�������ѧ���Ǻϳ�����ZԪ���γɵ�Z?������ʽΪ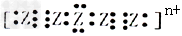 ����nֵ____________________��
����nֵ____________________��
��5��Z������������Ӧˮ�����������̬�⻯���ҷ�Ӧ�������α��� ?
�ټ�Ũ����Һ��YԪ�صĵ��ʹ��ȵĻ�ѧ��Ӧ����ʽΪ_____________________�� ?
�ڱ�?��ˮ�ĵ�����____________���ã�����ơ������ٽ�����Ӱ�족����ԭ���ǣ������ӷ���ʽ��ʾ��_______________________________��
����һ�������£����ҷ���̶��ݻ�����?��������ʹ�䷢���ֽⷴӦ����֪?���ﵽƽ��״̬�ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���___________��ѡ����ĸ��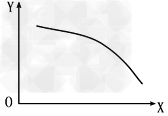
a����X��ʾ�¶�ʱ��Y��ʾ�ҵ����ʵ���
b����X��ʾѹǿ?ʱ��Y��ʾ�ҵ�ת����
c����X��ʾ��Ӧʱ��ʱ��Y��ʾ���������ܶ�
��6����X�ĵ��ʵ�ȼ����ΪM?KJ?����д���䵥���ڿ�����ȼ�յ��Ȼ�ѧ����ʽ��__________________________��
4��ѡ���� �ء��١�������Ԫ��λ�����ڱ���ͬһ���ڣ����ǵ����������ֱ�Ϊ���������������������������������Ԫ��ԭ�������Ĵ�С˳��Ϊ��������
A.��>��>��
B.��>��>��
C.��>��>��
D.��>��>��
5���ƶ��� �������ֶ�����Ԫ��X��Y��Z��W����֪��
��X��Wԭ�ӵĵ��Ӳ���������������֮�ȷֱ�Ϊ3��1��1��3��
��Yԭ����Ԫ�����ڱ���ԭ�Ӱ뾶��С��ԭ�ӣ�
��Z���� �ɻ�������������Ԫ�ء�
�ش��������⣺
(1)XԪ�������ڱ��е�λ����________��
(2)��������Ԫ���У�ֻ��һ��Ԫ�ص�ԭ�ӹ��ɵ�������_________�������ӷ��ţ���
(3)������X2W2�ĵ���ʽ��_________��
(4)��1molNa2SiO3����Һ�л���ͨ��2mol��ZW2����Ӧ�����ӷ���ʽ��________��
(5)��Y��Z��WԪ���е����ֻ����ֿ�����ɶ������ʣ����к���18�����ӵķ�����________���ѧʽ����
(6)��KMnO4��Һ����ͨ���ζ����ⶨY2Z2W4��Һ�����ʵ����ʵ���Ũ�ȡ���25.00mL��Y2Z2W4��Һ�м��� 5.00mL0.50mol/L����KMnO4��Һ��ǡ����ȫ��Ӧ���õ�ZW2��Mn2+�����Y2Z2W4��Һ�����ʵ����ʵ���Ũ����________mol/L��