时间:2017-07-27 08:48:40
1、填空题 (1)对于Ag2S(s) 2Ag+(aq)+ S2-(aq),其Ksp=____________。
2Ag+(aq)+ S2-(aq),其Ksp=____________。
(2)下列说法不正确的是__________。
A. 用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
B. 物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的;
C. 对于Al(OH)3(s)  Al(OH)3(aq)
Al(OH)3(aq) Al3++3OH-,前者为溶解平衡,后者为电离平衡;
Al3++3OH-,前者为溶解平衡,后者为电离平衡;
D. 除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大
E. 沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全。
参考答案:(1)[c(Ag+)]2·c(S2-)
(2)BD
本题解析:
本题难度:一般
2、简答题 已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A.AgCl>AgI>Ag2CrO4
B.AgCl>Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI
D.Ag2CrO4>AgI>AgCl
参考答案:A、由Ksp计算可知,Ag+浓度大小顺序应为Ag2CrO4>AgCl,故A错;
B、Ag+浓度大小顺序应为Ag2CrO4>AgCl,故B错;
C、饱和溶液中:对应化学式相似的AgCl和AgI来说Ksp越小Ag+浓度越小,即AgCl>AgI;Ag2CrO4溶液中Ag+的浓度为34.0×10-12
本题解析:
本题难度:一般
3、选择题 已知25℃时,AgI饱和溶液中c(Ag+)为1. 23×10-8 mol /L,AgCl的饱和溶液中c(Ag+)为1. 25×10-5 mol/L。若在5mL 含有KCl和KI各为0.01 mol/L的溶液中,逐滴加入5 mL 0.01 mol/L AgNO3溶液形成浊液,下列叙述正确是
[? ]
A.加入AgNO3溶液时首先生成AgCl沉淀
B.AgI的溶度积(Ksp)为1.23×10-10
C.浊液中Cl-和I-浓度之比约为1. 03×106
D.如果不考虑水的蒸发,升高温度,则浊液中沉淀的质量不变
参考答案:C
本题解析:
本题难度:一般
4、填空题 难溶性杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水中存在如下溶解平衡:
K2SO4·MgSO4·2CaSO4·2H2O(s) 2Ca2++2K++Mg2++4SO42-+2H2O。为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下:
2Ca2++2K++Mg2++4SO42-+2H2O。为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下: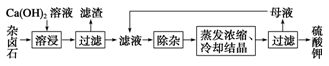
(1)滤渣主要成分有________和CaSO4以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
。
(3)“除杂”环节中,先加入 溶液,经搅拌等操作后,过滤,再加入 溶液调滤液pH至中性。
(4)不同温度下,K+的浸出浓度与溶浸时间的关系见右图。由图可得,随着温度升高,
① ,
② ,
③溶浸出的K+的平衡浓度增大。
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+CO32- CaCO3(s)+SO42-。已知298 K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,计算此温度下该反应的平衡常数,K= 。
CaCO3(s)+SO42-。已知298 K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,计算此温度下该反应的平衡常数,K= 。
参考答案:(1)Mg(OH)2(1分) (2)加入Ca(OH)2溶液,Mg2+与OH-结合生成Mg(OH)2沉淀,Mg2+浓度减小,平衡正向移动,K+增多(2分) (3)K2CO3(1分) H2SO4(1分)
(4)①溶浸平衡向右移动(1分) ②K+的溶浸速率增大(1分) (5) K=1.75×104。(2分)
本题解析:(1)“呆矿”在水中存在沉淀溶解平衡K2SO4·MgSO4·2CaSO4·2H2O(s) 2Ca2++2K++Mg2++4SO42-+2H2O,为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,氢氧根离子和镁离子结合生成氢氧化镁沉淀,同时钙离子增多,析出硫酸钙沉淀,所以滤渣中主要成分为Mg(OH)2和CaSO4以及未溶杂卤石。
2Ca2++2K++Mg2++4SO42-+2H2O,为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,氢氧根离子和镁离子结合生成氢氧化镁沉淀,同时钙离子增多,析出硫酸钙沉淀,所以滤渣中主要成分为Mg(OH)2和CaSO4以及未溶杂卤石。
(2)Ca(OH)2溶液能溶解杂卤石浸出K+的原因是氢氧化钙是饱和溶液,加入后氢氧根离子和镁离子结合生成氢氧化镁沉淀,促进平衡右移,增多K+。
(3))“除杂”环节主要是除去钙离子,依据除杂原则不能引入新的杂质,根据制取的目的是制备硫酸钾,所以加入的试剂易于除去,不引入新的杂质,因此加入过量K2CO3除钙离子,过滤后加入硫酸至中性,除去碳酸钾即可。
(4)分析不同温度下,K+的浸出浓度与溶浸时间的关系,温度越高K+的浸出浓度越大,溶浸时间越短,反应速率越大,达到平衡越快,故图象中分析得到的结论为:①溶浸平衡向右移动;②K+的溶浸速率增大。
(5)溶浸过程中会发生反应CaSO4(s)+CO32- CaCO3(s)+SO42-,CaCO3(s)
CaCO3(s)+SO42-,CaCO3(s) Ca2++CO32-;CaSO4(s)
Ca2++CO32-;CaSO4(s) Ca2++SO42-;依据硫酸钙、碳酸钙溶度积常数的计算表达式,转化关系中钙离子相同计算,反应的平衡常数K=
Ca2++SO42-;依据硫酸钙、碳酸钙溶度积常数的计算表达式,转化关系中钙离子相同计算,反应的平衡常数K=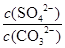 =
=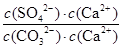 =
=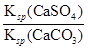 =
=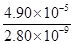 =1.75×104。
=1.75×104。
考点:考查溶解平衡的应用、判断以及溶度积常数的计算等
本题难度:困难
5、选择题 25℃ CaCO3固体溶于水达饱和时物质的量浓度是9.327×10-5 mol/L,则CaCO3在该温度下的Ksp为(?)
A.9.3×10-5 mol/L
B.9.7×10-9 mol2/L2
C.7.6×10-17 mol4/L4
D.8.7×10-9 mol2/L2
参考答案:D
本题解析:CaCO3饱和溶液中[Ca2+]=[CO32-]=9.327×10-5 mol/L,Ksp=[Ca2+]·[CO32-]=9.327×10-5 mol/L×9.327×10-5 mol/L=8.7×10-9 mol2/L2。
本题难度:一般