时间:2017-07-27 08:43:36
1、简答题 某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此得出的结论是浓硝酸的氧化性强于稀硝酸.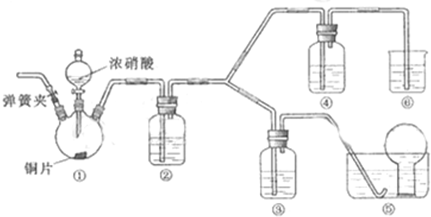
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是______
(2)滴加浓硝酸之前先检验装置的气密性,再加入药品;打开弹簧夹后______
(3)装置①中发生反应的化学方程式是______
(4)装置②的作用是______,发生反应的化学方程式是______
(5)该小组得出的结论依据的试验现象是______.
参考答案:(1)根据装置特点和实验目的,装置⑤是收集NO,装置⑥中盛放NaOH溶液吸收NO2防止污染大气;因为要验证稀HNO3不能氧化NO,所以装置③中应该盛放稀硝酸.
故答案为:3mol/L稀硝酸、浓硝酸、氢氧化钠溶液;
(2)由于装置中残存的空气能氧化NO而对实验产生干扰,所以滴加浓HNO3之前需要通入一段时间CO2赶走装置中的空气,同时也需将装置⑤中导管末端伸入倒置的烧瓶内防止反应产生的NO气体逸出.
故答案为:通入CO2一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内;
(3)Cu与浓HNO3反应生成Cu(NO3)2、NO2、H2O,反应为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,
故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
(4)装置②中盛放H2O,使NO2与H2O反应生成NO:3NO2+H2O=2HNO3+NO,故答案为:将NO2转化为NO;3NO2+H2O=2HNO3+NO;
(5)NO通过稀HNO3溶液后,若无红棕色NO2产生,说明稀HNO3不能氧化NO,所以盛放稀HNO3装置的液面上方没有颜色变化即可说明之.装置④中盛放的是浓HNO3,若浓HNO3能氧化NO则装置④液面的上方会产生红棕色气体,
故答案为:装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色.
本题解析:
本题难度:一般
2、选择题 已知2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2,H2S + I2 =" 2HI" + S,下列叙述正确的是( )
A.氧化性:Fe3+>I2>S
B.氧化性:I2>S>Fe3+
C.还原性:Fe2+>I->H2S
D.还原性:Fe2+>H2S>I-
参考答案:A
本题解析:根据氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物可推得。氧化性:Fe3+>I2>S;而还原性:Fe2+<I-<H2S
本题难度:一般
3、选择题 在浓盐酸中H3AsO3与SnCl2反应的离子方程式为3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62―+6M。下列关于该反应的说法中,错误的是( )
A.M为H2O
B.每还原1 mol氧化剂,就有3 mol电子转移
C.还原性:SnCl2>As
D.氧化产物和还原产物的物质的量之比为2∶3
参考答案:D
本题解析:根据原子守恒可知M为H2O,A项正确;Sn由+2价升高到+4价,SnCl2作还原剂,As由+3价降低到0价,H3AsO3作氧化剂,转移3 mol电子,B、C项正确;氧化产物和还原产物的物质的量之比为3∶2,D项错误
本题难度:一般
4、选择题 氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO=bO2↑+cCl2↑+dHClO4+eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法正确的是
[? ]
A.物质HClO4的氧化性大于HClO3的氧化性
B.若化学计量数a=8,b=3,则8 mol氯酸分解转移电子数为20NA
C.变蓝的淀粉碘化钾试纸褪色可能是发生反应:4Cl2+I2+ 6H2O=12H++8Cl-+2IO3-
D.氯酸分解所得O2和Cl2的物质的量之比是确定不变的
参考答案:B
本题解析:
本题难度:简单
5、选择题 甲、乙代表2种金属,下列叙述中,不能判断金属活动性甲比乙强的是
A.常温下,甲能从水中置换出氢,而乙不能
B.最高价氧化物对应的水化物碱性比较,甲比乙的强
C.甲与非金属反应时失电子比乙少
D.甲、乙作电极,稀硫酸为电解质溶液组成原电池,乙电极表面产生气泡
参考答案:C
本题解析:A.在金属活性性顺序表中,活泼的金属能把水会酸中是H置换出来,而活动性弱的金属不能把水或酸中是H置换出来,因此能作为判断金属活动性甲比乙强的依据。正确。B.元素的金属性越强,其最高价氧化物对应的水化物碱性就越强,元素的金属性越弱,其最高价氧化物对应的水化物的碱性就越弱。因此可以作为比较甲比乙的金属性强的依据。正确。C.要比较金属活动性的强弱,应该看金属原子失去电子的难易,而不是金属原子失去电子的多少,因此不能作为判断金属活性性强弱的依据。错误。D.一般情况下,有活动性不同的金属与电解质溶液形成原电池时,活动性强的金属作负极,发生氧化反应;活动性弱的金属作正极,在正极上发生还原反应。所以甲、乙作电极,稀硫酸为电解质溶液组成原电池,乙电极表面产生气泡,能证明活动性甲>乙。正确。
本题难度:一般