时间:2017-07-27 08:43:14
1、填空题 (12分)某研究性学习小组探究醋酸的溶液情况,进行了如下实验。
(1)取一定量的冰醋酸配制250 mL 0.5000 mol・L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、___________和___________。
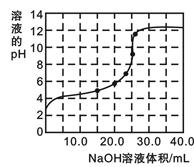
(2)用上述0.5000 mol・L-1的醋酸溶液再进行稀释,为测定稀释后醋酸溶液的准确浓度,用0.2000 mol・L-1的NaOH溶液对25.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 25.05 | 25.00 | 23.80 | 24.95 |
2、简答题 ①常温下,有0.1mol/L的盐酸和0.1mol/L的醋酸溶液,比较两溶液的pH,盐酸______(填“<”、“=”或“>”)醋酸,写出醋酸电离的方程式______.
②测得某溶液的pH=6.5,且氢离子与氢氧根离子物质的量相等,此溶液呈______性.测定温度______室温(填高于、低于或等于),其理由是______.
3、选择题 下列各组物质的水溶液中,溶质分子与其离子之间存在电离平衡的是? (? )
A.氨水、氯水
B.HNO3、H2SO4
C.Ba(OH)2和BaSO4
D.醋酸、酒精
4、选择题 现有常温下的五种溶液(如下表)。
| ? | ① | ② | ③ | ④ | ⑤ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 | 醋酸钠 |
| pH | 11 | 11 | 3 | 3 | 8.3 |
5、选择题 在18 ℃时,H2SO3的K1=1.5×10-2、K2=5.0×10-7,H2CO3的K1=1.4×10-7、K2=2.7×10-11,则下列说法中正确的是 (? )
A.多元弱酸的酸性主要由第一步电离决定,亚硫酸的酸性弱于碳酸
B.多元弱酸的酸性主要由第二步电离决定,碳酸的酸性弱于亚硫酸
C.多元弱酸的酸性主要由第一步电离决定,亚硫酸的酸性强于碳酸
D.多元弱酸的酸性主要由第二步电离决定,碳酸的酸性强于亚硫酸