时间:2017-07-27 08:13:53
1、选择题 常温下甲、乙两醋酸溶液,测得甲的pH= a,乙的pH= a+1。下列推断中正确的是
A.甲中由水电离产生的H+的物质的量浓度是乙的0.1倍
B.物质的量浓度c(甲)=10c(乙)
C.中和等物质的量的NaOH溶液,需甲、乙两酸的体积V(乙)>10V(甲)
D.甲中的c(OH-)为乙中的c(OH-)的10倍
2、选择题 下列溶液中加入少量NaOH固体导电能力变化不大的是( )
A.NH3・H2O
B.CH3COOH
C.盐酸
D.H2O
3、选择题 下表是常温下某些一元弱酸的电离常数:
| 弱酸 | HCN | HF | CH3COOH | HNO2 |
| 电离常数 | 6.2×10-10 | 6.8×10-4 | 1.8×10-5 | 6.4×10-4 |
4、选择题 向0.1mol/L CH3COOH溶液中加入CH3COONa晶体或加等体积水稀释时,都会引起
[? ]
A.溶液的pH增大
B.CH3COOH的电离程度增大
C.溶液的导电能力减小
D.溶液的c(OH-)减小
5、简答题 常温下,浓度均为0.1mol/L的四种溶液:①Na2CO3溶液?②NaHCO3溶液?③盐酸?④氨水
试回答下列问题:
(1)上述溶液中有水解反应发生的是______(填编号,下同),溶液中溶质存在电离平衡的是______;
(2)比较①、②溶液,pH值较大的是______;
(3)在溶液④中加入少量NH4Cl固体,此时C(NH4+)/C(OH-)的值将______(填“变小”、“变大”或“不变”);
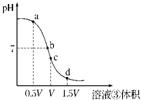
(4)用溶液③滴定V?mL溶液④其滴定曲线如图所示:
①试分析在滴定过程中,滴定曲线上a、b、c、d四点,水的电离程度最大的是______点,理由是______;
②a点溶液中离子浓度大小关系是______;
③取少量c点溶液于试管,再滴加0.1mol/L?NaOH溶液至中性.此时溶液中除H+、OH-外,离子浓度大小关系是______.