时间:2017-07-18 02:39:40
1、填空题 (6分)写出下列物质在水溶液中的电离方程式或离子水解方程式。
1、写出下列三种物质的电离方程式
(1) HClO 。
(2)CH3COONa 。
(3)NH3・H2O 。
2、写出下列三种物质的离子水解方程式
(4)CH3COONa 。
(5)NH4Cl 。
(6)NaF 。
2、填空题 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | HA物质的量 浓度(mol・L-1) | NaOH物质的量 浓度(mol・L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | C1 | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
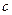 (A-)与
(A-)与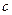 (Na+)的大小关系是?。
(Na+)的大小关系是?。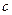
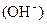 =?mol・L-1。
=?mol・L-1。3、选择题 体积相同,pH相同的 ①稀盐酸 ②稀硫酸 ③稀醋酸,分别用同物质的量浓度的NaOH溶液完全中和时,所消耗的NaOH溶液的体积关系正确的是
A.②=①>③
B.②>①>③
C.②<①=③
D.③>②=①
4、选择题 下列说法中,能说明酸HA的酸性比酸HB的酸性强的是
A.同温、同浓度的钠盐溶液PH:NaA>NaB
B.PH相同的HA,HB的酸溶液,稀释相同倍数后,PH:HA<HB
C.中和等体积、等PH的HA,HB溶液时,HA消耗NaOH的物质的量多
D.同温、同浓度的两种酸溶液,HA的电离程度大于HB的电离程度
5、选择题 把0.05mol NaOH固体分别加入到100mL下列溶液中,溶液的导电能力变化最小的是
A.自来水
B.0.5mol・L-1盐酸
C.0.5mol・L-1醋酸溶液
D.0.5mol・L-1KCl溶液