时间:2017-07-18 01:50:17
1、选择题 R2O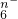 在一定条件下可以把Mn2+氧化成MnO
在一定条件下可以把Mn2+氧化成MnO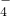 ,若反应后R2O
,若反应后R2O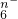 转变为RO
转变为RO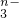 .又知反应中氧化剂与还原剂的物质的量之比为5:2,则n值为
.又知反应中氧化剂与还原剂的物质的量之比为5:2,则n值为
A.1
B.2
C.3
D.4
2、填空题 北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g) CH4(g)+HC≡CH(g)+H2(g);△H1="156.6" kJ・mol-1
CH4(g)+HC≡CH(g)+H2(g);△H1="156.6" kJ・mol-1
CH3CH=CH2(g) ?CH4(g)+HC=CH(g);△H2="32.4" kJ・mol-1
?CH4(g)+HC=CH(g);△H2="32.4" kJ・mol-1
则相同条件下,反应C3H8(g) ?CH3CH=CH2(g)+H2(g)的△H=_____kJ・mol-1
?CH3CH=CH2(g)+H2(g)的△H=_____kJ・mol-1
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应方程式为___________;放电时,CO32-移向电池的_______(填“正”或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol・L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3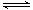 HCO3- +H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
HCO3- +H+的平衡常数K1=_____________。(已知:10-5.60=2.5×10-6)
(4)常温下,则溶液c(H2CO3)______c(CO32-)(填“>”、“=”或“<”),原因是_______________________(用离子方程式和必要的文字说明)。
3、填空题 下表为元素周期表的一部分:
| 族 周期 | | | | |||||
| 1 | ① | | | | | | | |
| 2 | | | | | | ② | | |
| 3 | ③ | | | ④ | | ⑤ | ⑥ | |

4、填空题 (15分)
化合物AX3和单质X2在一定条件下反应可生成化合物AX5。回答下列问题:
(1)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成lmol AX5,放出热量123.8 kJ。该反应的热化学方程式为 。
(2)反应AX3(g)+X2(g) AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。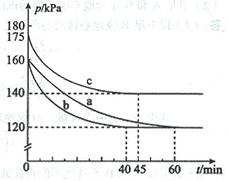
①列式计算实验a从反应开始至达到平衡时的反应速率 v(AX5)= 。
②图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为 (填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:b 、
c 。
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为
;实验a和c的平衡转化率:αa为 、αc为 。
5、选择题 实验室由MnO2和浓盐酸制取纯净的氯气时,气体通过两个洗气瓶,第二个洗气瓶应盛(?)
A.稀盐酸
B.浓硫酸
C.水
D.饱和食盐水