时间:2017-07-10 20:08:57
1、选择题 制备HCl气体,下列方法可行的是
①NaHSO4+MnCl2(固)共热?②浓H2SO4+浓HCl共热
③浓H2SO4+KCl(固)共热?④浓H2SO4+NaCl(固)+MnO2共热
A.①③
B.①②③
C.①③④
D.全部
参考答案:B
本题解析:略
本题难度:简单
2、选择题 根据相似相溶的一般规律,若要溶解NaCl应选用
[? ]
A.水
B.CCl4
C.酒精
D.汽油(非极性分子)
参考答案:A
本题解析:
本题难度:简单
3、简答题 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与族序数相等,请回答下列问题:
| Q | R | T W |
参考答案:T所处的周期序数与族序数相等,应为第三周期第ⅢA族元素Al,根据元素所在周期表中的位置可知Q为C,R为N,W为S元素,则
(1)T为Al,为周期表13号元素,原子核外有3个电子层,最外层电子数为3,原子结构示意图为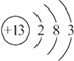
,
故答案为:
;
(2)根据S、C最高价氧化物对应的酸性硫酸强于碳酸,则可得非金属性S强于C,故答案为:<;
(3)S与浓H2SO4发生反应,从元素守恒看,肯定有水生成,另外为一气体,从化合价和性质看,只能是SO2,则反应的化学方程式为S+2H2SO4(浓)?△?.?3SO2↑+2H2O,
故答案为:S+2H2SO4(浓)?△?.?3SO2↑+2H2O;
(4)比R质子数多1的元素为O,存在H2O2转化为H2O的反应,反应的化学方程式为2H2O2?MnO2?.?2H2O+O2↑,
故答案为:2H2O2?MnO2?.?2H2O+O2↑;
(5)12g碳是1mol,燃烧生成1molCO2,与1.5molNaOH反应的化学方程式为:2CO2+3NaOH=NaHCO3+Na2CO3,生成碳酸钠、碳酸氢钠各0.5mol,溶液中大量存在的离子有Na+、HCO3-、CO32-,故答案为:Na+、HCO3-、CO32-.
本题解析:
本题难度:一般
4、选择题 下列化合物中,既有离子键,又有非极性共价键的是( )
A.Na2O2
B.NH3
C.NH4Cl
D.HCl
参考答案:A
本题解析:
本题难度:一般
5、选择题 X、Y、Z三种短周期元素在周期表中的位置如下图所示.若X的最高正价与负价的代数和为2,则下列说法正确是( )
A.原子序数由大到小为Z>Y>X
B.氢化物最稳定的元素为Z
C.最高价氧化物的水化物酸性最强的元素为Z
D.原子半径由大到小为Z>Y>X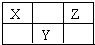
参考答案:由X、Y、Z三种短周期元素在周期表中的位置可知,X、Z处于第二周期,Y处于第三周期,若X的最高正价与负价的代数和为2,则X处于ⅤA族,故X为氮元素、Z为氟元素、Y为硫元素,
A.X为氮元素、Z为氟元素、Y为硫元素,原子序数Y>Z>X,故A错误;
B.F元素的非金属性最强,HF最稳定,故B正确;
C.F元素没有含氧酸,故C错误;
D.同周期自左而右原子半径减小,电子层越多原子半径越多,故原子半径S>N>F,故D错误;
故选B.
本题解析:
本题难度:简单