时间:2017-07-10 20:02:41
1、选择题 A、B、C三种短周期元素在周期表中位置如图示,B位于ⅥA族.下列叙述错误的是( )
A.原子半径大小顺序为B>A>C
B.非金属性强弱顺序为B>C>A
C.BO2与H2B在常温下可发生反应
D.A的氢化物水溶液呈碱性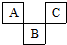
参考答案:B
本题解析:
本题难度:一般
2、选择题 右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
A.常压下五种元素的单质中,Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物的沸点比X的氢化物的沸点高
D.Y元素的非金属性比W元素的非金属性强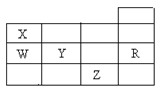
参考答案:D
本题解析:
本题难度:简单
3、填空题 将下列物质:①CH4、②Ar、③NH3、④MgO、⑤SiO2、⑥NaOH、⑦NH4Cl按要求填空
(1)微粒间只存在共价键的是___________,只存在离子键的是___________,既存在离子键,又存在共价键的是___________。
(2)属于离子化合物的是___________,其中只有离子键的化合物的电子式为___________。
(3)属于共价化合物的是___________。
参考答案:(1)CH4、NH3、SiO2;MgO;NaOH、NH4Cl
(2)MgO、NaOH、NH4Cl;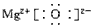
(3)CH4、NH3、SiO2
本题解析:
本题难度:一般
4、填空题 氮可以形成多种离子,如N3-、NH2-、NH2、N3、NH4+、N2H5+、N2H62+等,已知N2H5+与N2H62+是由中 性分子结合质子形成的,类似于NH4+,因此有类似于NH4+的性质。
(1)写出N2H62+与足量的NaOH溶液反应的离子方程式:___。
(2)N2O、CO2、CNO -都与N3-互为等电子体,它们具有相似的结构,则请写出N3-的电子式为___。
(3)据报道,美国科学家卡尔・克里斯特于1998年11月合成了一种阳离子“N5n+”,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N三N键。请写出 “N5n+”带具体电荷的电子式和结构式:___、____。
(4)请你预计科学家即将合成的N8属于___(填“单质”、“共价化合物”或“离子化合物”);其电子式为___,请写出其含有的所有化学键的类型:___;预计它在常温下是___体,熔沸点__(填“低”、“较高”或“高”),熔融状态下___(填“会”或“不会”)导电。
参考答案:(1)N2H62+ +2OH+=N2H4 +2H2O
(2)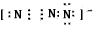
(3)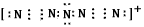 ;
;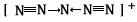
(4)单质; ;离子键、非极性共价键、配位键;固;较高;会
;离子键、非极性共价键、配位键;固;较高;会
本题解析:
本题难度:一般
5、选择题 下列化合中,只含有共价键的是( ? )
A.H2O
B.CaO
C.NaCl
D.NaOH
参考答案:A
本题解析:
本题难度:简单