时间:2017-07-10 19:39:46
1、选择题 已知常温下反应①NH3+H+ NH
NH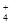 (平衡常数为K1),②Ag++Cl-
(平衡常数为K1),②Ag++Cl-
参考答案:
本题解析:
本题难度:一般
2、选择题 实验:①0.1 mol/L AgNO3溶液和0.1 mol/L NaCl溶液等体积混合得到浊液,过滤。
②分别取少量①的滤液,分别滴加等浓度等体积的饱和Na2S溶液、饱和Na2SO4溶液,前者出现浑浊,后者溶液仍澄清。
③取少量①的沉淀,滴加几滴氨水,沉淀逐渐溶解。
下列分析不正确的是
A.实验②证明了①的滤液中含有Ag+,由此推断①的滤液中也含有Cl¯
B.实验②证明了该温度下Ag2S比Ag2SO4更难溶解
C.实验③的溶液中含有Ag(NH3)2+微粒
D.由实验③推测:若在①的沉淀中滴加NaOH溶液,沉淀也能溶解
参考答案:D
本题解析:A、实验②滴加饱和Na2S溶液出现浑浊,证明了①的滤液中含有Ag+,根据电荷守恒可由此推断①的滤液中也含有Cl¯,A正确;B、实验②证明了该温度下Ag2S比Ag2SO4更难溶解,B正确;C、实验③的溶液生成银氨溶液,含有Ag(NH3)2+微粒,C正确;D、由实验③推测:使沉淀溶解是因为含有氨生成了银氨溶液,不是与氢氧根离子反应,D错误;答案选D。
考点:离子反应、溶解沉淀平衡
本题难度:困难
3、选择题 将足量的AgI分别放入下列物质中,AgI的溶解度由大到小的排列顺序是(?)
①5mL0.001mol・L-1KI溶液?②15mL0.002mol・L-1CaI2溶液?
③35mL0.003mol・L-1HI溶液?④15mL蒸馏水?⑤45mL0.005mol・L-1AgNO3溶液
A.①>②>③>④>⑤
B.④>①>③>②>⑤
C.⑤>④>②>①>③
D.④>③>⑤>②>①
参考答案:B
本题解析:根据碘化银的溶解平衡可知,只有降低银离子或碘离子的浓度,才能促进碘化银的溶解。①~⑤中碘离子或银离子的浓度分别为(mol/L)0.001、0.004、0.003、0、0.005,所以答案B是正确的。答案选B。
本题难度:一般
4、选择题 下列说法正确的是( )
A.难 溶电解质的溶度积Ksp越小,则它的溶解度越小
溶电解质的溶度积Ksp越小,则它的溶解度越小
参考答案:
本题解析:
本题难度:一般
5、选择题 下列化学实验能达到目的是( )
A.用激光笔检验某KI溶液中是否溶有淀粉
B.加入适量溴水后过滤,可除去苯中的少量苯酚
C.向碘水中加入苯或酒精,均可从碘水中萃取碘
D.向AgCl沉淀中滴加少量KI溶液,可说明Ksp(AgCl)<Ksp?(AgI)
参考答案:A.KI溶液中溶有的淀粉是胶体,胶体有丁达尔现象,用激光笔检验,看到一条光亮的通路,说明含有淀粉,如不能说明没有淀粉,因碘化钾溶液没有丁达尔现象,故A正确;
B.溴易溶于苯,溴水与苯发生萃取,苯酚与溴水发生取代反应生成三溴苯酚,用溴水除杂,生成的三溴苯酚和过量的溴都能溶于苯,不能得到纯净的苯,并引入新的杂质,不能用来除杂,除去苯中的少量苯酚,应向混合物中加入NaOH溶液后分液,故B错误;
C.苯和水不互溶,且碘在苯中的溶解度大于在水中的溶解度,苯和碘不反应,所以苯能作萃取剂萃取碘水中的碘;酒精和水互溶,所以酒精不能作萃取剂,故C错误;
D.在AgCl饱和溶液中加入NaI固体,有AgI沉淀生成,说明AgI难溶,AgCl比AgI的溶度积常数大,故D错误;
故选A.
本题解析:
本题难度:简单