ʱ��:2017-07-10 18:43:13
1��ѡ���� �����йص���ʵĵ����ˮ��˵����ȷ���ǣ�?��
A����25��ʱ���κ�ˮ��Һ��Kw=1��10-14��
B����NaHSO4��Һ�У�c(H+)=c(OH-)+c(SO42-)
C����pH=2�������ữ��FeCl3��Һ��ϡ����10��������ҺpH=3
D��0.1mol/L������Һ�м�������ᣬƽ�������ƶ�������ĵ���̶�����
�ο��𰸣�B
���������A����25��ʱ�����κ����ʵ�ϡ��ˮ��Һ�д�����Kw=1��10-14�����Ũ�ȽϴͲ����ϡ�����B.����Һ��H+��H2O��NaHSO4��ͬ���������NaHSO4=Na++H++ SO42-.��H2O H++OH-.��c(H+)=c(OH-)+c(SO42-)����ȷ��C����pH=2�������ữ��FeCl3��Һ����ϡ����10��������ˮ��ij̶Ȳ�������ҺpH=3����ϡ��ʹFeCl3��ˮ��̶��������Һ2<pH<3.����D��0.1mol/L������Һ�м�������ᣬƽ�������ƶ����������ӵĴ����ƽ���ƶ����ٵĴ���Ҫ�࣬�ô���ĵ���̶ȷ�����С������
H++OH-.��c(H+)=c(OH-)+c(SO42-)����ȷ��C����pH=2�������ữ��FeCl3��Һ����ϡ����10��������ˮ��ij̶Ȳ�������ҺpH=3����ϡ��ʹFeCl3��ˮ��̶��������Һ2<pH<3.����D��0.1mol/L������Һ�м�������ᣬƽ�������ƶ����������ӵĴ����ƽ���ƶ����ٵĴ���Ҫ�࣬�ô���ĵ���̶ȷ�����С������
�����Ѷȣ�һ��
2��ѡ���� ���й���0.10 mol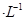 NaHSO3��Һ��˵����ȷ����
NaHSO3��Һ��˵����ȷ����
A������NaOH���壬��ҺpH��С
B���¶����ߣ�c(HSO3��)����
C��25 Cʱ����ˮϡ�ͺ�n(H��)��n��OH�����ij˻����
Cʱ����ˮϡ�ͺ�n(H��)��n��OH�����ij˻����
D��NaHSO3�ĵ��뷽��ʽΪNaHSO3 = Na��+H��+SO32-
�ο��𰸣�C
�������������NaHSO3+NaOH=Na2SO3+H2O������NaOH���壬��ҺPH����A�����HSO3-�ĵ�����̺�ˮ����̶������ȹ��̣��¶����ߣ������������ˮ��̶�����c(HSO3��)��С��B�������ͬһ��Һ�У�n(H��)?n(OH��)=C(H��)?c(OH��)V��V=KwV��V,��ˮϡ�ͣ�KW���䣬V�������ˮϡ�ͺ�n(H��)��n��OH�����ij˻����C����ȷ��������ǿ����ʣ����뷽��ʽΪNaHSO3 = Na��+HSO3-��D�����ѡC��
���㣺����NaHSO3��Һ�и��ֹ�ϵ��
�����Ѷȣ�һ��
3��ѡ���� ��֪����ʱ��0.1mo1/LCH3COOH��ˮ����0.1%�������룬����������ȷ���ǣ�������
A������Һ��pH=5
B�������¶ȣ���Һ��pH����
C��CH3COOH�ĵ���ƽ�ⳣ��ԼΪ1��10-6
D����CH3COOH�������c��H+��ԼΪˮ�������c��H+����106��
�ο��𰸣�A��HA�������c��H+��Ϊ0.1mol/L��0.1%=10-4mol/L����pH=-lg��10-4��=4����A����
B���¶����ߴٽ�����ĵ��룬������Ũ�ȱ����pH��С����B����
C����HA�TH++Ac-��c��H+��=c��Ac-��=10-4mol/L�������ƽ�ⳣ��Ϊ=[H+][Ac-]HAc=10-4��10-40.1=1��10-7����C����
D��HA�������c��H+��Ϊ0.1mol/L��0.1%=10-4mol/L��ˮ���������������Ũ��Ϊ10-10mol/L������HA�������c��H+��ԼΪˮ�������c��H+����106������D��ȷ��
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� ������Һ�д��ڵ���ƽ��CH3COOH H����CH3COO����������������ȷ���ǣ�?��
H����CH3COO����������������ȷ���ǣ�?��
A��������Һ������Ũ�ȵĹ�ϵ���㣺c��H������c��OH������c��CH3COO����
B��0��10mol/L��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c��OH������С
C��CH3COOH��Һ�м�������CH3COONa���壬ƽ�������ƶ�
D��������pH��2��CH3COOH��Һ��pH��12��NaOH��Һ�������Ϻ���Һ��pH��7
�ο��𰸣�B
���������A���ڴ�����Һ�д��ڵ���������H������������OH����CH3COO�������ݵ���غ��֪��������Һ������Ũ�ȵĹ�ϵ���㣺c��H������c��OH������c��CH3COO��������ȷ��B��0��10mol/L��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c��H������С����������Һ�д���Kw=c��H������c��OH����������c��OH����������C�� ������Һ�д��ڵ���ƽ��CH3COOH H����CH3COO����������CH3COONa���壬c(CH3COO��)������ƽ���ƶ�ԭ���������������Ũ�ȣ�ƽ���������ƶ�����ȷ��D������CH3COOH�����ᣬ���ֵ��룬��NaOH��ǿ���ȫ���롣�ڳ�����pH��2��CH3COOH��Һ��pH��12��NaOH��Һ���������c��H������c��OH����=10��2mol/L���������Ϻ����H+ǡ����ȫ���кͣ���ʱ�ƻ��˴���ĵ���ƽ�⣬���������������H����CH3COO��ֱ���ﵽ�µ�ƽ�⣬���ڴ�ʱ��Һ��c��H����>c��OH����������pH��7����ȷ��
H����CH3COO����������CH3COONa���壬c(CH3COO��)������ƽ���ƶ�ԭ���������������Ũ�ȣ�ƽ���������ƶ�����ȷ��D������CH3COOH�����ᣬ���ֵ��룬��NaOH��ǿ���ȫ���롣�ڳ�����pH��2��CH3COOH��Һ��pH��12��NaOH��Һ���������c��H������c��OH����=10��2mol/L���������Ϻ����H+ǡ����ȫ���кͣ���ʱ�ƻ��˴���ĵ���ƽ�⣬���������������H����CH3COO��ֱ���ﵽ�µ�ƽ�⣬���ڴ�ʱ��Һ��c��H����>c��OH����������pH��7����ȷ��
�����Ѷȣ�һ��
5������� ��12�֣������г��������¼ס��ҡ���������Һ����Ϊ0.1 mol��L��1��NaOH��Һ����Ϊ0.1 mol��L��1��HCl��Һ����Ϊ0.1 mol��L��1��CH3COOH��Һ���Իش��������⣺
��1������Һ��pH��________��
��2������Һ�д��ڵ���ƽ��Ϊ______________________(�õ���ƽ�ⷽ��ʽ��ʾ)��
��3���ס��ҡ���������Һ����ˮ�������c(OH��)�Ĵ�С��ϵΪ_________��
��ijһԪ����(��HA��ʾ)��ˮ�еĵ��뷽��ʽ��HA
�ο��𰸣�
���������
�����Ѷȣ�һ��