时间:2017-07-10 18:21:37
1、选择题 如表是不同pH环境时某浓度铬酸(H2CrO4)溶液中,离子浓度(mol/L)与pH的关系,下列说法错误的是( )
| pH | c(CrO42-) | c(HCrO4-) | c(Cr2O72-) | c(H2CrO4) 4 0.0003 0.1040 0.4480 0 6 0.0319 0.0999 0.4370 0 7 0.2745 0.0860 0.3195 0 9 0.9960 0.0031 0.0004 0 |
参考答案:A.由表中数据可知铬酸溶液中不含H2CrO4,说明铬酸的第一步电离是完全电离,则铬酸第一级电离方程式为H2CrO4=H++HCrO4-,故A错误;
B.根据表中数据知,pH越大,电离出的CrO42- 浓度越大,所以要得到CrO42-应控制溶液的pH>9,故B正确;
C.溶液中存在2CrO4 2-+2H+?CrO72-+H2O,当电离达到平衡状态时,2v逆(Cr2O72-)=v正(CrO42-),故C错误;
D.在pH=4时,c(CrO42-),=0.0003mol/L,c(HCrO4-)=0.1040mol/L,c(Cr2O72-)=0.4480mol/L,所以铬酸溶液的物质的量浓度约为1.00mol/L,故D正确;
故选AC.
本题解析:
本题难度:一般
2、选择题 某种碳酸饮料中主要含柠檬酸、碳酸、白砂糖、苯甲酸钠等成分,常温下测得其pH约为3.5,下列说法不正确的是
A.柠檬酸的电离会抑制碳酸的电离
B.该碳酸饮料中水的电离受到抑制
C.常温下,该碳酸饮料中KW的值大于纯水中KW的值
D.打开瓶盖冒出大量气泡,是因为压强减小,降低了CO2的溶解度
参考答案:C
本题解析:A、柠檬酸电离生成H+,抑制碳酸的电离,正确;B、酸电离出的H+抑制水的电离,正确;C、KW受温度的影响,与溶质无关,所以常温下,该碳酸饮料中KW的值等于纯水中KW的值,错误;D、压强减小,气体的溶解度降低,正确。
本题难度:一般
3、选择题 下列溶液中,相关微粒的浓度关系正确的是
A.MgSO4溶液:c(Mg2+)+c(H+)=" c" (SO42一)+c(OH一)
B.将0.2mol・L-1CH3 COOH溶液与0.1mo1・L-1NaOH溶液等体积混合:c(CH3 COO一)+ c(CH3COOH)=2c(Na+)
C.将pH=2的盐酸与0.01 mo1・L-1氨水等体积混合:c(NH4+)=" c" (Cl一)
D.由AgCl和AgI固体混合物与水形成的悬浊液:c(Ag+)>c(Cl一) =" c" (I一)
参考答案:B
本题解析:A.MgSO4溶液中根据电荷守恒可知2c(Mg2+)+c(H+)=2c(SO42一)+c(OH一),A错误;B.将0.2mol・L-1CH3 COOH溶液与0.1mo1・L-1NaOH溶液等体积混合生成醋酸钠和水,同时醋酸过量。所得溶液是醋酸钠和醋酸的混合液,且二者的浓度相等,根据物料守恒可知c(CH3 COO一)+ c(CH3COOH)=2c(Na+),B正确;C.pH=2的盐酸其浓度是0.01mol/L,且盐酸是强酸,因此与0.01 mo1・L-1氨水等体积混合后恰好反应生成氯化铵,铵根水解溶液显酸性,则c(NH4+)<c(Cl一),C错误;D.由于氯化银和碘化银的溶度积常数不同,则由AgCl和AgI固体混合物与水形成的悬浊液中氯离子浓度不等于碘离子浓度,D错误,答案选B。
考点:考查溶液中离子浓度大小比较
本题难度:一般
4、选择题 已知某温度下,几种酸的电离常数如下:Ka(HCN)= 6.2×10-10 mol/L、Ka(HF)= 6.8×10-4 mol/L、Ka(CH3COOH)= 1.8×10-5 mol/L、Ka(HNO2)= 6.4×10-6mol/L。则物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是
A.NaCN
B.NaF
C.CH3COONa
D.NaNO2
参考答案:B
本题解析:由这几种弱酸在相同温度下的电离平衡常数可以判断酸性:HF> CH3COOH > HNO2> HCN。酸越弱,相同条件下相同浓度的其相应的Na盐水解程度越大,溶液的碱性就越强,PH就越大。故物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是NaF。选项为:B.
本题难度:一般
5、选择题 25℃时,将水不断滴入0.1 mol/L的氨水中,下列变化的图像不正确的是
[? ]
A.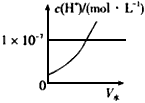
B.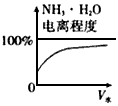
C.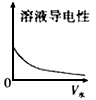
D.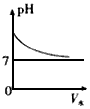
参考答案:A
本题解析:
本题难度:一般