时间:2017-03-05 16:05:09
1、实验题 某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。某化学课外小组设计以下流程,以该矿样为原料生产CuCl2?2H2O晶体。
已知:在20℃时,氯化铜的溶解度是73g;常温下,金属离子开始沉淀和沉淀完全时的pH见下表。
| 金属离子 | 开始形成氢氧化物沉淀的pH | 完全形成氢氧化物沉淀的pH |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |

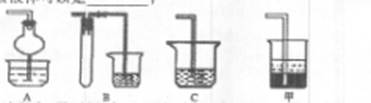
参考答案:(1)2H2O2 = 2H2O+O2↑,2Na2O2 + 2H2O= 4NaOH+O2↑
(2)AB?四氯化碳
(3)100ml容量瓶、量筒
(4)调节溶液的pH,使Fe3+以Fe(OH)3沉淀的形式析出? A
(5)3
本题解析:(1)根据装置图可知是固液不加热制气体,所以用H2O2和Na2O2来制取O2反应方程式为:2H2O2 = 2H2O + O2 ↑,2Na2O2 + 2H2O ="4NaOH" + O2 ↑
(2)尾气中含有的是SO2,SO2为酸性氧化物,极易溶于水,可由碱液吸收,但易形成倒吸,故可采用AB装置防倒吸:A中的干燥管可缓冲倒吸、B装置中的试管可做安全瓶;
若选用甲装置,可采用密度大于水的有机溶剂,例如四氯化碳,也可起到防倒吸的作用
(3)配制盐酸一般采取稀释的方法,用量筒量取一定的浓盐酸;
还需要选用100 mL容量瓶的容量瓶进行配制
(4)根据氢氧化物开始沉淀和完全沉淀的pH可知,只要调节pH值,就可以Fe3+以Fe(OH)3沉淀的形式析出,达到除杂的目的。为了不引入新杂质,还能调节pH值,所以选铜的难溶物,如CuO、Cu(OH)2、CuCO3等
(5)除了图示的两次过滤操作外,对CuCl2浓缩结晶后,还需要过滤才可得到产品,故共需要三次过滤操作
本题难度:一般
2、填空题 如图甲所示,某同学将一小块钠放在石棉网上加热,观察到生成的产物除了淡黄色固体外还有一些黑色固体物质,当时他想这种黑色物质应该是钠表面吸附的煤油不完全燃烧产生的碳单质,但在学习了镁与C02的反应后,该同学想:就金属活动性而言,Na比Mg还强,该黑色物质是否是Na与C02反应生成的碳单质。为了验证自己的想法,该同学利用装置乙进行实验。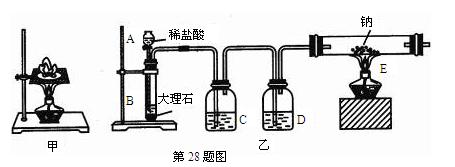
实验步骤如下:①切取一小块金属钠,用滤纸完全吸干煤油,再除去表面的氧化层,放进干燥的E中;
②打开分液漏斗的活塞,使B中的反应进行一段时间后,再点燃E处的酒精灯。
实验现象如下:钠在充满C02气体的玻璃管中剧烈燃烧起来,产生大量的白烟;玻璃管中有黑色物质生成;待玻璃管冷却后,管壁上附着一层白色物质。
请回答下列问题:
(1)C中盛放的试剂是?,作用是?。D中盛放的试剂是?,作用是?。
(2)B中的反应进行一段时间后,再点燃E处的酒精灯的目的是?。
(3)该同学将白色物质和黑色物质分别溶于水,发现黑色物质不溶于水,白色物质能溶于水。由此,该同学得出结论,该黑色物质是Na与C02反应生成的碳单质,则其他生成物还应该有?。
(4)请设计一实验方案验证玻璃管内Na与C02反应生成的白色物质的成分,并写出实验步骤、现象和结论?。
(5)若先点燃E处的酒精灯,再打开分液漏斗的活塞,写出此时玻璃管E中可能发生的反应的化学方程式?。
参考答案:(1)饱和NaHC03溶液?除去C02中的HCl气体?浓硫酸?除去C02中的水蒸气
(2)用C02排尽装置内空气?
(3)Na2 C03?
(4)取少量白色固体于试管 中,加入稀盐酸,如果产生无色无味
中,加入稀盐酸,如果产生无色无味 能使石灰水变浑浊的气体,则证明白色固体是碳酸钠?
能使石灰水变浑浊的气体,则证明白色固体是碳酸钠? ?
?
(5)
本题解析:略
本题难度:一般
3、选择题 下列实验方案合理的是
A.鉴别集气瓶中的甲烷和乙烯:分别点燃,观察火焰的颜色及是否有黑烟
B.检验酒精中的少量水:向酒精中加入足量生石灰
C.制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应
D.除去乙烷中的乙烯气体:将实验室制得的乙烯气体通入NaOH 溶液
参考答案:A
本题解析:A正确,甲烷中含碳量少,燃烧时火焰呈蓝色,乙烯中含碳量高些,燃烧时火焰明亮且伴有少量黑烟;
B错,检验酒精中的少量水:向酒精中加入白色的无水硫酸铜,若变蓝则说明有水存在。
C错,光照条件下发生取代反应的产物复杂,副产物多,通常制备卤代烃的方法是用烯烃的加成反应;
D错,乙烯与NaOH 溶液不反应,除去乙烷中的乙烯气体可将混合气体通入溴水。
本题难度:一般
4、实验题 (10分)中学化学中几种常见物质的转化关系如下:(提示:A单质有可变价态且与硫反应生成低价态)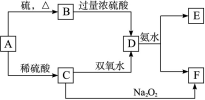
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体F粒子直径大小的范围:________。
(2)B的化学式:________。
(3)写出:D的溶液与氨水反应的离子方程式:
________________________________________________________________________;
C的溶液与双氧水反应的离子方程式:
________________________________________________________________________。
(4)写出鉴定E中阳离子的实验方法和现象:
________________________________________________________________________。
参考答案:(1)1~100 nm
(2)FeS
(3)Fe3++3NH3・H2O===Fe(OH)3↓+3NH 2Fe2++H2O2+2H+===2Fe3++2H2O
(4)取少量E溶液于一试管中,加入适量浓NaOH溶液,加热产生的气体能使湿润的红色石蕊试纸变蓝色,则证明溶液中含NH?
本题解析:由F为Fe(OH)3知A为Fe,B为FeS,C为FeSO4,D为Fe2(SO4)3,E为(NH4)2SO4。
本题难度:一般
5、选择题 下列实验中,合理的是
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.用100mL 量筒量取5.20mL 盐酸
C.用托盘天平称取25.20g NaCl固体
D.用100mL 容量瓶配制125mL 0.1mol・L-1盐酸
参考答案:A
本题解析:略
本题难度:简单