ʱ��:2017-03-05 14:47:15
1��ѡ���� ���и������ǿ����ʡ�������ʡ��ǵ���ʵĹ��࣬��ȫ��ȷ����(����)
| ? | A | B | C | D |
| ǿ����� | Fe | NaCl | CaCO3 | HNO3 |
| ������� | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
| �ǵ���� | C12H22O11(����) | BaSO4 | C2H5OH | H2O |
�ο��𰸣�C
������������Ȳ��ǵ���ʣ�Ҳ���Ƿǵ���ʣ�A�����NH3�Ƿǵ���ʣ�BaSO4��ǿ����ʣ�B�����̼������Σ�Ϊǿ����ʣ���������ǿ�ᣬ��������ʣ��Ҵ��Ƿǵ���ʣ�C����ȷ��H2O��������ʣ�D�����
�����Ѷȣ���
2������� ��5�֣������£�������һԪ�ᣨHX��HY��HZ���ֱ��NaOH��Һ�������ϣ�ʵ���������£�
| �� | c(һԪ��) /mol��L�C1 | c(NaOH) /mol��L�C1 | �����Һ��pH |
| HX | 0.1 | 0.1 | pH = x |
| HY | 0.1 | 0.1 | pH = 7 |
| HZ | 0.1 | 0.1 | pH = 9 |
�ο��𰸣���5�֣���1��HY?
��2��HZ +OH- ="=" H2O + Z-�� H2O + Z-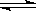 HZ+OH-
HZ+OH-
��3��10x-14?C
�����������1�������ʵ����������������ƻ�ϣ���Һ�������ȡ�������ǿ����������ǿ�ᣬ����Һ�����ԣ����������ᣬ����Һ�ʼ��ԣ�����������������һ������ǿ�����HY��
��2����HZ���������ƻ��Һ��pH�ж�HZ�����ᣬ�������ӷ���ʽʱ���ܲ��������ʽ���������ӷ���ʽΪHZ +OH- ="=" H2O + Z-��������Һ��pH����7��ԭ������ΪZ-ˮ��ʹ��Һ�ʼ��ԣ�ˮ������ӷ���ʽΪH2O + Z-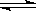 HZ+OH-
HZ+OH-
��3��HX������������Һ��Ӧ�����Һ��pH=x������Һ�е�c(H+)=10-xmol/L����Һ�е�c(OH-)=10x-14 mol/L��HX��Ϊǿ�����ҺΪ������Һ����Ϊ���ᣬ�����ҺΪ������Һ��������Һ�е�OH-��Ũ�ȼ���ˮ���������OH-��Ũ�ȣ�c(OH-)=10x-14 mol/L���������Ϸ�����x�R7����ѡC��
�����Ѷȣ�һ��
3������� ����һƿŨ��Ϊ0.2 mol/L��ij����Һ������Ϊ���ᡢ���ᡢ�����е�һ�֡�Ϊ��ȷ��������Һ����ɽ���ʵ�飺ȡ25.00 mL0.1 mol/L������������Һ����μ��������Һ��ǡ�÷�Ӧ��ȫʱ���������Һ���Ϊ12.50 mL����ش�
��1�����������__________��
��2����pH��ֽ��÷�Ӧ��������Һ�ʼ��ԣ����ݴ�����˵��������ҺΪ__________�������ӷ���ʽ˵����Һ�ʼ��Ե�ԭ��__________________��
��3��ʵ���еζ�������ͼ�� 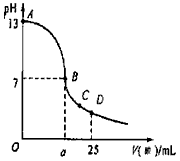
��B�㣬a_______12.5������ڡ�С�ڻ���ڣ���C�������Ũ���ɴ�С����_________________��
�ο��𰸣���1������
��2�����CH3COO-+H2O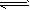 CH3COOH+OH-
CH3COOH+OH-
��3�����ڣ�c(CH3COO-) >c(Na+) > c(H+)>c(OH-)
���������
�����Ѷȣ�һ��
4��ѡ���� ����ͼʾ���Ӧ������һ����ȷ����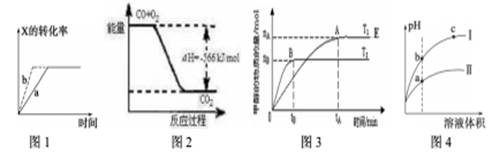
A��ͼ1��ʾ����ӦX��g��+2Y��g��3Z��g����b��ѹǿһ����a��
B��ͼ2��ʾCO����CO2�ķ�Ӧ���̺�������ϵ
C��ͼ3��ʾ��ӦCO��2H2CH3OH,�����¶�T1>T2,�������������������£�������E�����ϵ�����ѹ����ԭ����1/2��ƽ�������ƶ�������Ũ������
D��ͼ4��ʾ����ˮϡ��pH��ͬ������ʹ��ᣬI��ʾ���ᣬII��ʾ���ᣬ����Һ������c>b>a
�ο��𰸣�C
������������ڸ÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ����������������ѹǿ����ʹ�ô�������ѧƽ�ⶼ���ƶ������b��ѹǿ��һ����a��A����ͼ2��ʾCO��ѹǿ��������CO2�ķ�Ӧ���̣����ڷ�Ӧ���������������ߣ����Ը÷�Ӧ�Ƿ��ȷ�Ӧ��B�ԡ���ͼ�����¶���T1ʱ���ȴﵽƽ�⣬���������¶Ȼ�ѧ��Ӧ���ʼӿ죬��֪�¶�T1>T2, �������������������£�������E�����ϵ�����ѹ����ԭ����1/2������������ϵ��ѹǿ����������Ӧ�����������С�ķ�Ӧ����������ѹǿ��ƽ�������ƶ�������ƽ���ƶ������������ģ��ܵ���˵����Ũ��������C�ԡ���ˮϡ��pH��ͬ������ʹ��ᣬ���ڴ��������ᣬ����Һ�д��ڵ���ƽ�⣬���Բ�����Һ�����ӵ�Ũ�ȱ仯С��pH�仯ҲС������I��ʾ���ᣬII��ʾ���ᣬ��Һ��pHԽ������Ũ�Ⱦ�ԽС����Һ�ĵ���������Խ����������Һ������c<b<a,D����
�����Ѷȣ�һ��
5��ѡ���� �����й�˵����ȷ����
A��CaCO3(s)=CaO(s)��CO2(g)�����²����Է����У�˵���÷�Ӧ�ġ�H��0
B����������Һ�еμӷ�̪�Ժ�ɫ��֤������Ϊ�������
C��N2(g)��3H2(g) 2NH3(g) ��H��0��������������ʱ�����¶ȣ���Ӧ����v(H2)��������ƽ��ת���ʾ�����
2NH3(g) ��H��0��������������ʱ�����¶ȣ���Ӧ����v(H2)��������ƽ��ת���ʾ�����
D��ij�¶��£���ˮ�е�c(H+)=1.0��10-6.5mol/L������¶���pH=1��������ˮ�����c(H+)=1.0��10-12mol/L
�ο��𰸣�BD
���������A��CaCO3(s)=CaO(s)��CO2(g)����ϵ���ҳ̶�����ķ�Ӧ���������²����Է����У�˵���÷�Ӧ�ġ�H>0������B�����������Σ�������Һ�еμӷ�̪�Ժ�ɫ��֤����������ǿ�������Σ���������ӷ���ˮ�ⷴӦ����ˮ���������c(H+),����Һ��c(OH-)> c(H+)�����Դ���Ϊ������ʣ���ȷ��C��N2(g)��3H2(g) 2NH3(g) ��H��0��������������ʱ�����¶ȣ���Ӧ����v(H2)�ӿ죻�����¶ȣ�����ƽ���ƶ�ԭ����ƽ�������ȵķ����ƶ����Ը÷�Ӧ��˵��ƽ�������ƶ�������������ƽ��ת���ʼ�С������D��ij�¶��£���ˮ�е�c(H+)=1.0��10-6.5mol/L��Kw=1.0��10-13mol2/L2�������¶ȸ������¡�����¶���pH=1��������ˮ�����c(H+)= c(OH-)=1.0��10-13mol2/L2��1.0��10-1mol/L=1.0��10-12mol/L������
2NH3(g) ��H��0��������������ʱ�����¶ȣ���Ӧ����v(H2)�ӿ죻�����¶ȣ�����ƽ���ƶ�ԭ����ƽ�������ȵķ����ƶ����Ը÷�Ӧ��˵��ƽ�������ƶ�������������ƽ��ת���ʼ�С������D��ij�¶��£���ˮ�е�c(H+)=1.0��10-6.5mol/L��Kw=1.0��10-13mol2/L2�������¶ȸ������¡�����¶���pH=1��������ˮ�����c(H+)= c(OH-)=1.0��10-13mol2/L2��1.0��10-1mol/L=1.0��10-12mol/L������
���㣺���鷴Ӧ���Է��ԡ��ε�ˮ�⡢��ѧƽ�⼰������ʵĵ����֪ʶ��
�����Ѷȣ�һ��