时间:2017-03-05 14:31:09
1、填空题 1840年盖斯根据一系列实验事实得出规律,他指出:“若是一个反应可以分步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同。”这是在各反应于相同条件下完成时的有关反应热的重要规律,称为盖斯定律。已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:
C(金刚石、s)+O2(g)=CO2(g);△H=-395.41kJ/mol,
C(石墨、s)+O2(g)=CO2(g);△H=-393.51kJ/mol,
则金刚石转化石墨时的热化学方程式为:__________________________。由此看来更稳定的碳的同素异形体为:____________。若取金刚石和石墨混合晶体共1mol 在O2中完全燃烧,产生热量为QkJ,则金刚石和石墨的物质的量之比为_____________(用含Q的代数式表示)。
参考答案:C(金刚石、s)=C(石墨、s) △H=-1.90kJ/mol;石墨;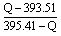
本题解析:
本题难度:一般
2、选择题 已知: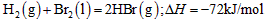 蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表
蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表
参考答案:D
本题解析:
本题难度:一般
3、选择题 金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石并需要吸收能量。已知12g石墨或金刚石完全燃烧时放出的热量依次为Q1和Q2,下列说法错误的是
[? ]
A.Q1< Q2
B.石墨不如金刚石稳定
C.石墨具有的能量比金刚石低
D.石墨与金刚石完全燃烧,生成的二氧化碳一样多
参考答案:B
本题解析:
本题难度:一般
4、选择题 已知25℃、101 kPa时:
4Al(s) +3O2(g)=2Al2O3(s) △H=-2835 kJ/mol
4Al(s)+2O3(g)=2Al2O3(s) △H=-3119 kJ/mol
下列说法正确的是
[? ]
A.O3比O2稳定,由O2转化为O3是吸热反应
B.O2比O3稳定,由O2转化为O3是放热反应
C.等质量的O2比O3能量高,由O2转化为O3是放热反应
D.等质量的O2比O3能量低,由O2转化为O3是吸热反应
参考答案:D
本题解析:
本题难度:一般
5、选择题 已知:
2Zn(s)+O2(g)=2ZnO(s)△H1=-702.2kJ/mol?
2Hg(s)+O2(g)=2Hg?O(s)△H2=-181.4kJ/mol
Zn(s)+HgO(s)=Hg(s)+ZnO(s)△H3
则△H3的值是( ? )
A.-441.8kJ/mol
B.-254.6kJ/mol
C.-438.9kJ/mol
D.-260.4kJ/mol
参考答案:D
本题解析:
本题难度:一般