ʱ��:2017-03-05 14:22:54
1������� (1)�(PH3)��һ����ɫ�о綾�����壬�仹ԭ�����Ȱ�(NH3)ǿ����һ��ǿ��ԭ����ij��Ӧ��ϵ�д����������ʣ�Cu��H2SO4��CuSO4��PH3��H3PO4��H2O��
�ش��������⣺
��������Ӧ��ϵ�л�ѧ��Ӧ����ʽΪ________________��
���(PH3)�ܺ�ˮ�������Ļ�ѧ��Ӧ����ˮ��Һ�������ԣ��÷�Ӧ�������ӷ���ʽ��ʾΪ___________________��
(2)������ˮ�к�����ϸС��������ɼ���ijЩ����ʹ֮�ۼ��ɽϴ�Ŀ����������������һ�ֳ�������ʹ������ˮ��������۳������ʣ��仯ѧʽΪ________________
(3)��CH4����ԭNOx�������������������Ⱦ�����磺
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H2
��1 mol CH4��ԭNO2��N2�����������зų�������Ϊ867 kJ�����H2=___________��
�ο��𰸣�(1) ��PH3+4CuSO4+4H2O=4Cu+H3PO4+4H2SO4����PH3+H2O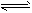 PH4++OH-����PH3+ H2O
PH4++OH-����PH3+ H2O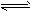
PH3��H2O��PH3��H2O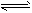 PH4++OH-��
PH4++OH-��
(2)KAl(SO4)2��12H2O
(3)-1160 kJ��mol-1
���������
�����Ѷȣ�һ��
2������� ��֪�����Ȼ�ѧ����ʽ��
��2H2��g��+O2?��g��=2H2O��l������H=-570kJ?mol-1
��2H2��g��+O2?��g��=2H2O��g������H=-483.6kJ?mol-1
��C��s��+
| 1 2 |
�ο��𰸣���1�������Ȼ�ѧ����ʽ��2H2��g��+O2 ��g��=2H2O��l������H=-570kJ?mol-1��
���ȼ���ȵĸ����������õ�������ȼ���ȵ��Ȼ�ѧ����ʽΪ��H2��g��+12O2 ��g��=H2O��l������H=-285kJ?mol-1��
�ʴ�Ϊ��285KJ/mol��
��2��ȼ��1gH2����Һ̬ˮ���ų�������Ϊx�����������Ȼ�ѧ����ʽ���㣺
? 2H2��g��+O2 ��g��=2H2O��l������H=-570kJ?mol-1
? 4g? 570KJ
? 1g? x
x=142.5KJ��
�ʴ�Ϊ��142.5KJ��
��3�������Ȼ�ѧ����ʽ����C��s��+12O2 ��g��=CO��g������H=-110.5kJ?mol-1����C��s��+O2 ��g��=CO2��g������H=-393.5kJ?mol-1 ��
���ݸ�˹���ɢ�-�۵õ���CO��g��+12O2��g��=CO2��g����H=-283KJ/mol
�ʴ�Ϊ��CO��g��+12O2��g��=CO2��g����H=-283KJ/mol��
���������
�����Ѷȣ�һ��
3������� ��֪�����Ȼ�ѧ����ʽ��
��H2��g��+1/2O2��g����H2O��l���� ��H=-285 kJ��mol-1
��H2��g��+1/2O2��g����H2O��g���� ��H=-241��8 kJ��mol-1
��C��s��+1/2O2��g�� ��CO��g���� ��H=-110��5 kJ��mol-1
��C��s��+O2��g�� ��CO2��g���� ��H=-393��5 kJ��mol-1
�ش��������⣺
��1��H2��ȼ����Ϊ______________��C��ȼ����Ϊ______________��
��2��ȼ��1gH2����Һ̬ˮ���ų�������Ϊ______________��
��3��д��COȼ�յ��Ȼ�ѧ����ʽ______________��
�ο��𰸣���1��285KJ/mol��393.5KJ/mol
��2��142.5KJ
��3��CO��g��+1/2O2 ��g����CO2��g����H����283KJ/mol
���������
�����Ѷȣ�һ��
4������� �ҹ��Ǹ������������������Ϊ�����һ����¯��������Ϊ�ձ��������������¯�ڿ��ܷ������·�Ӧ��
C(s)+O2(g)=CO2(g) ��H1=-393.5 kJ/mol ��
C(s)+CO2(g)=2CO(g) ��H2=+172.5 kJ/mol ��
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) ��H3=-13.7 kJ/mol ��
��ش��������⣺
(1)��Ӧ3Fe(s)+2O2(g)=Fe3O4(s)�ġ�H=_____________��
(2)800��ʱ��C(s)+CO2(g)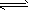 2CO(g)��ƽ�ⳣ��K=1.64����ø�¯��c(CO)= 0. 20 mol/L��c(CO2)=
2CO(g)��ƽ�ⳣ��K=1.64����ø�¯��c(CO)= 0. 20 mol/L��c(CO2)=
0.05mol/L����ʱ��Ӧ��____����������桱��������С�
(3)ij�ֿ�ʯ����Ԫ����������FemOn��ʽ���ڣ���ʯ�����ʲ����ᷴӦ�����ֽ�������ʵ�飺����������ʯ��Ʒ���飬��ȡ25��0 g��Ʒ���ձ��У�����ϡH2SO4����ܽ⣬�����ϼ��ȡ����裬��ȥ�������������Һ�м���10��0 gͭ�۳�ַ�Ӧ����ˡ�ϴ�ӡ������ʣ�����36 g��ʣ����Һ��Ũ��Ϊ2
mol/L������KMnO4�ζ������յ�ʱ����KMnO4��Һ���25��0 mL����ʾ��2Fe3++Cu=2Fe2++Cu2+
8H++MnO4-+5Fe2+=Mn2++5Fe3++4H2O
�ټ��������ʯ����Ԫ�ص�����������
�ڼ���������FemOn�Ļ�ѧʽ��m��nΪ������������д��������̣���
�ο��𰸣�(1) -1118. 3 kJ/mol
(3)�ٽ�:n(Fe)=5n(KMnO4)=50.025L��2mol/L=0. 25mol
m(Fe)=0.25mol��56g/mol=14g
��(Fe)=14g/25g��100%=56%
�ڷ�Ӧ��ͭ�����ʵ���n(Cu)=(10g-3.6g)/64g/mol=0.1mol
�ɷ���ʽ�ã�n(Fe3+)=0.2 mol��n(Fe2+)=0.05 mol
��������Ļ�ѧʽ�ɱ�ʾΪ��Fe5O7��FeO��Fe2O3
���������
�����Ѷȣ�һ��
5������� ��ú��Ϊȼ�Ͽ�ͨ����������;����
;��I��C��s��+O2��g���TCO2��g����H1��0��
;��II�����Ƴ�ˮú����C��s��+H2O��g���TCO��g��+H2��g����H2��0��
��ȼ��ˮú����2CO��g��+O2��g���T2CO2��g����H3��0��
2H2��g��+O2��g���T2H2O��g����H4��0��
��ش��������⣺
��1��;��I�ų�������______������ڡ������ڡ���С�ڡ���;��II�ų���������
��2����H1����H2����H3����H4����ѧ��ϵʽ��______��
��3��12g̿���������в���ȫȼ������һ����̼���ų�110.35kJ���������Ȼ�ѧ����ʽΪ______��
�ο��𰸣���1���ɸ�˹���ɿ�֪������һ����Ӧ���Էֲ����У��������Ӧ�����ջ�ų��������ܺ��������Ӧһ�η���ʱ���ջ�ų���������ͬ���ʴ�Ϊ�����ڣ�
��2�����ݸ�˹���ɣ���Ӧ1=��Ӧ2+��Ӧ3��12+��Ӧ4��12���ԡ�H1=��H2+12����H3+��H4�����ʴ�Ϊ����H1=��H2+12����H3+��H4����
��3��12g̿���������в���ȫȼ������һ����̼���ų�110.35kJ��������1mol̿���������в���ȫȼ������һ����̼���ų�110.35kJ�������Ȼ�ѧ����ʽΪ��C��s��+12O2��g��=CO��g����H=-110.35kJ?mol-1���ʴ�Ϊ��C��s��+112O2��g��=CO��g����H=-110.35kJ?mol-1��
���������
�����Ѷȣ���