时间:2017-03-05 14:12:58
1、选择题 将一元酸HA的溶液与一元碱BOH的溶液等体积混合,若所得溶液呈酸性,下列有关判断正确的是
A.若混合前酸、碱物质的量浓度相同,则HA肯定是弱酸
B.溶液中水的电离程度:混合溶液>纯水>BOH溶液
C.若混合前酸、碱pH之和等于14,则HA肯定是弱酸
D.混合溶液中离子浓度一定满足:c(B+)>c(A-)>c(H+)>c(OH-)
参考答案:C
本题解析:A中酸碱恰好反应,水解显碱性,不正确。由于无法判断,酸碱的过量,所以选项B不一定正确。C正确,此时酸是过量的,因此显酸性。根据电荷守恒可知c(B+)+c(H+)=c(A-)+c(OH-),所以选项D是不可能的,答案选C。
本题难度:简单
2、填空题 25时,如果取0.1 mol・L-1HA溶液与0.1 mol・L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因是 (用离子方程式表示);
(2)混合溶液中由水电离出的c(H+)__ ___0.1 mol・L-1 NaOH溶液中由水电离出的c(H+);(选填“>”、“<”、或“=”)
(3)求出混合液的下列算式的精确计算结果(填具体数字):c(Na+)-c (A-)= mol・L-1;
(4)已知NH4A溶液是中性,又知将HA溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的
pH 7(选填“>”、“<”或“=”);
(5)将相同温度下浓度相同的四种盐溶液:
A.NH4HCO3
B.NH4A
C.(NH4)2SO4
D.NH4Cl
按pH由大到小的顺序排列 (填序号)
参考答案:(1)A-+H2O HA+OH-(2)> (3)9.9×10-7 (4)> (5)ABDC
HA+OH-(2)> (3)9.9×10-7 (4)> (5)ABDC
本题解析:(1)若HA是强酸,则恰好生成强酸强碱盐,溶液显中性,而溶液PH=8,说明溶液显碱性,生成的是强碱弱酸盐,水解显碱性。(2)盐类水解促进水的电离,酸、碱都能抑制水的电离,所以混合溶液中由水电离出的c(H+)>0.1 mol・L-1,NaOH溶液中由水电离出的c(H+)。(3)本小题考查的是电荷守恒问题和有关pH的计算,c(Na+)+c(H+)=c(OH-)+ c(A),所以c(Na+)-c(A)=c(OH)-c(H+)=1×10-6mol・L-1-1×10-8mol・L-1。根据质子守恒A-+H2O HA+OH-和H2O
HA+OH-和H2O H++OH-可知OH-有两个来源,c(OH-)= c(H+)+ c(HA),c(OH-)-c(HA)=c(H+)=1×10-8mol・L-1。(4)已知将HA溶液加到Na2CO3溶液中有气体放出,说明HA比H2CO3的酸性强,HA比H2CO3的电离程度大,NH4A溶液呈中性,HA的电离程度与氨水的电离程度相当,所以氨水的电离程度比H2CO3的电离程度大,(NH4)2CO3溶液的pH>7。(5)根据水解规律可知H2CO3的电离程度最弱,故NH4HCO3溶液显碱性,其pH最大,NH4A 溶液显中性,H2SO4、HCl都是强酸溶液显酸性,但(NH4)2SO4中c(NH4+)的值大,酸性最强,pH最小。
H++OH-可知OH-有两个来源,c(OH-)= c(H+)+ c(HA),c(OH-)-c(HA)=c(H+)=1×10-8mol・L-1。(4)已知将HA溶液加到Na2CO3溶液中有气体放出,说明HA比H2CO3的酸性强,HA比H2CO3的电离程度大,NH4A溶液呈中性,HA的电离程度与氨水的电离程度相当,所以氨水的电离程度比H2CO3的电离程度大,(NH4)2CO3溶液的pH>7。(5)根据水解规律可知H2CO3的电离程度最弱,故NH4HCO3溶液显碱性,其pH最大,NH4A 溶液显中性,H2SO4、HCl都是强酸溶液显酸性,但(NH4)2SO4中c(NH4+)的值大,酸性最强,pH最小。
考点:盐类水解,
本题难度:困难
3、选择题 下列液体均处于25°C,有关叙述正确的是
A.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
B.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐
C.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中的100倍
D.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-)
参考答案:C
本题解析:A、在同浓度的CaCl2和NaCl溶液中,铝离子浓度较大,对氯化银的溶解起到了抑制作用,所以AgCl在同浓度的CaCl2和NaCl溶液中的溶解度不相同,错误;B、pH<7的溶液有可能是酸,强酸弱碱盐或者强酸的酸式盐,错误;C、pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中的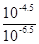 =100倍,正确;D、pH=5.6的CH3COOH与CH3COONa混合溶液中,c(CH3COO-)>c(Na+),错误;故本题选择C。
=100倍,正确;D、pH=5.6的CH3COOH与CH3COONa混合溶液中,c(CH3COO-)>c(Na+),错误;故本题选择C。
考点:难溶电解质的溶解平衡,pH的基本计算,离子浓度的比较
本题难度:一般
4、填空题 (1)已知在常温下测得浓度均为0.1 mol/L的下列5种溶液的pH: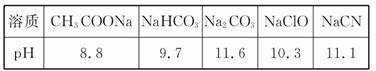
根据上述信息判断,浓度均为0.05 mol/L的下列5种物质的溶液中,pH最小的是 (填编号);其pH为 (填数值);pH最大的是 (填编号)。
①CH3COOH ②HCN ③HClO ④H2SO4 ⑤HClO4
(2)下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液。
②在侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体。
③蒸发KCl和NaNO3混合溶液,首先析出NaCl晶体。
根据上述反应,总结出复分解反应发生的一个规律: ;
将KI溶液和AgCl固体混合搅拌,会观察到的现象是 ,
请写出反应的离子方程式: 。
参考答案:(1)④ 1 ②
本题解析:(1)5种溶液中H2SO4、HClO4为强酸,相同浓度时H2SO4的pH最小,pH=-lg(2×0.05)=1。pH最大的即酸性最弱的,根据“酸越弱越水解”并结合题干信息,相同浓度时NaCN碱性强,则对应的HCN的酸性最弱,pH最大。因CO32-对应酸为HCO3-,此处易将Na2CO3溶液碱性更强误认为H2CO3酸性最弱。
(2)从题给3个转化可以看出,反应之所以能够发生,是因为生成溶解度更小的物质。因AgI的溶解度小于AgCl,白色沉淀AgCl能够转化为黄色沉淀AgI
本题难度:一般
5、填空题 (6分)在25℃时,将酸HA与碱MOH等体积混合.
(1)若0.01mol/L的强酸HA与0.01mol/L强碱MOH混合,则所得溶液显 (填“酸性”、“中性”或“碱性”,下同)该反应的离子方程式为 。
(2)若PH=3的强酸HA与PH=11的弱碱MOH混合,则所得溶液显 ,
理由是 。
(3)若0.01mol/L的强酸HA与0.01mol/L弱碱MOH混合,则所得溶液显 ,解释这一现象的离子方程式是 。
参考答案:(1)中性 H++OH-=H2O(2)碱性 酸HA与碱MOH中和后,碱过量,还会电离出OH-
(3)酸性 M++H2O MOH+H+
MOH+H+
本题解析:(1)等浓度的一元强酸与一元强碱等体积混合,恰好反应生成强酸强碱盐,该盐溶液显中性,该反应的离子方程式为H++OH-=H2O;
(2)强酸电离出的H+浓度等于弱碱电离出的OH-,所以弱碱的浓度大于强酸,则等体积混合后溶液为强酸弱碱盐和弱碱的混合溶液,显碱性,原因是酸HA与碱MOH中和后,碱过量,还会电离出OH-;
(3)同浓度的一元强酸与一元弱碱等体积混合,恰好反应生成强酸弱碱盐,溶液呈酸性,出现这一现象的离子方程式M++H2O MOH+H+。
MOH+H+。
考点:考查溶液的酸碱性,溶液的PH,酸碱中和反应等知识。
本题难度:一般