时间:2017-03-05 14:01:30
1、选择题 NH4HCO3是一种离子化合物,下列关于该物质的叙述错误的是( )
A.所含四种元素的原子半径由小到大的顺序为:H<O<N<C
B.同周期的三种元素的得电子能力由大到小的顺序为:O>N>C
C.除去NaCl固体中混有少量的NH4HCO3固体可以采用加热的方法
D.其与足量氢氧化钠溶液共热的离子方程式为:NH4++OH-
参考答案:A.C、N、O位于相同周期,同周期元素从左到右,原子半径逐渐减小,则半径由小到大的顺序为:H<O<N<C,故A正确;
B.同周期元素从左到右元素的非金属性逐渐增强,则得电子能力由大到小的顺序为:O>N>C,故B正确;
C.碳酸氢铵加热易分解,生产环氨气、二氧化碳和水,可用加热的方法除杂,故C正确;
D.与足量氢氧化钠溶液共热生成氨气、碳酸钠和水,反应的离子方程式为HCO3-+NH4++2OH-△
本题解析:
本题难度:简单
2、选择题 下列气态氢化物中最稳定的是( )
A.CH4
B.SiH4
C.H2S
D.HCl
参考答案:对于C、Si、S、Cl四种非金属元素来说,Si、S、Cl处于同一周期,同周期从左到右元素的非金属性增强,即非金属性Si<S<Cl;
C和Si处于同一主族,同主族从上到下非金属性减弱,即非金属性C>Si.对C和Cl来说,可以形成CCl4,说明Cl得电子能力比C强,即非金属性Cl>C.
综合上述分析,C、Si、S、Cl四种非金属元素中Cl的非金属性最强,即其氢化物HCl在CH4、SiH4、H2S、HCl中最稳定.
故选D.
本题解析:
本题难度:简单
3、选择题 下列说法正确的是( ? ?)
A.原子半径大小:Na>S>O
B.金属性强弱:K>Na>Ca
C.酸性强弱:HIO4>HBrO4>HClO4
D.碱性强弱:LiOH>NaOH>KOH
参考答案:A
本题解析:
本题难度:简单
4、推断题 A,B,C,D4种元素,A单质在B单质中燃烧发出苍白色火焰,C单质跟A,D形成化合物的水溶液反应生成A单质,C原子与B原子的电子层结构相同,且最外层电子数之差为奇数,D原子最外层电子数为K层电子数的3倍,其单质为淡黄色固体。
(1)4种元素的符号分别为A______,B______,C______,D______;
(2)离子的电子层结构相同的2种元素是_________,离子的结构示意图分别为________、_______;
(3)4种元素中能形成AB型共价化合物的元素是_____________,由它们的同位素原子形成的AB型分子
共有____________,其中质量数最小的一种分子可用同位素符号表示为____________;
(4)A,B,C,D原子形成的最高价氧化物的化学式分别为____,____,____,____。
参考答案:(1)H;Cl;Mg;S
(2)Cl;S; ;
;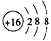
(3)HCl;6种;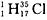
(4)H2O;Cl2O7;MgO;SO3
本题解析:
本题难度:一般
5、选择题 若已发现了116号元素,则下列叙述中正确的是①其钠盐的分子式为Na2R;②其最高价氧化物的水化物是强酸;③R是金属元素;④R是非金属元素;⑤其最高价氧化物的分子式为RO3( )
A.①③⑤
B.②④
C.③⑤
D.②③⑤
参考答案:如第七周期排满,最后一种元素的元素序数为118,为0族元素,则116号元素R位于ⅥA族,为氧族元素,原子最外层电子数为6,最高正价为+6价,
①116号元素为金属元素,不能与Na形成化合物,故①错误;
②同主族元素从上到下元素的非金属性逐渐减弱,金属性逐渐增强,其最高价氧化物的水化物应呈碱性,故②错误;
③同主族元素从上到下元素的金属性逐渐增强,第六周期元素为Po,属于金属元素,则116号元素肯定为金属元素,故③正确;
④由③分析可知R为金属元素,故④错误;
⑤R位于ⅥA族,为氧族元素,原子最外层电子数为6,最高正价为+6价,则其最高价氧化物的分子式为RO3,故⑤正确,
故③和⑤正确.
故选C.
本题解析:
本题难度:一般