时间:2017-03-05 13:49:59
1、选择题 将0.1L含有0.02mol?CuSO4和0.01mol?NaCl的水溶液用惰性电极电解.电解一段时间后,某电极的质量增加了0.64g.下列说法正确的是( )
A.质量增加的电极为阳极
B.电解过程中电子转移数为0.02NA
C.电解过程中某电极上只有Cl2产生
D.电解过程中pH增大
参考答案:0.1L含有0.02mol CuSO4和0.01mol NaCl的水溶液用惰性电极电解,阴极反应发生Cu2++2e-→Cu,电解一段时间后,某电极的质量增加了0.64g,即析出0.01molCu,则转移0.02mol电子,阳极反应为:2Cl-→2e-+Cl2↑,只有0.01mol的Cl-,所以只能转移0.01mol电子,生成0.005mol的氯气,阳极上接着放电的是氢氧根离子,即4OH-→4H2O+O2↑+4e-,还要转移0.01mol电子,当转移0.01mol电子时,生成氧气的物质的量是0.0025mol,所以阳极上生成的气体有0.005mol的氯气和0.0025mol的氧气,
A.阴极反应为Cu2++2e-→Cu,质量增加的为阴极,故A错误;
B.某电极的质量增加了0.64g,即析出0.01molCu,则转移0.02mol电子,故B正确;
C.由以上分析可知电极生成的气体为氯气和氧气,故C错误;
D.由于发生4OH-→4H2O+O2↑+4e-,促进水的电离,则电解过程中pH减小,故D错误.
故选B.
本题解析:
本题难度:简单
2、选择题 (2014届浙江省宁波市十校高三3月联考理综化学试卷)
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
A.铁是阳极,电极反应为Fe-6e一+4H2O=FeO42-+ 8H+
B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
C.若隔膜为阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
参考答案:D
本题解析:
A项中,铁是阳极,但溶液是碱性,不可能生成8H+,不正确;B项中,电解时电子的流动方向为:负极→Ni电极,溶液中是离子导电,再是Fe电极→正极,故不正确;C项中,因阳极消耗OH-,故OH-通过阴离子交换膜自左向右移动,C不正确; D项中,电解时阳极吸引OH-而使附近的pH降低、阴极区因OH-向右侧移动而pH升高;因为总反应消耗OH-,撤去隔膜混合后,与原溶液比较pH降低,说法正确。
本题难度:一般
3、选择题 如图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜,一段时间后停止通电,A池D极产生的气体在标准状况下为2.24 L。下列说法正确的是(?)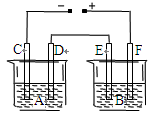
A.A池为电解池,B池为原电池
B.D电极与E电极都发生氧化反应
C.F极是以粗铜板为材料作阳极
D.B池中E极质量增加25.6 g
参考答案:C
本题解析:由图可以知道,AB池都是电解池,所以A选项错误;在电解池中,与电池的正极连接的为阳极,发生了氧化反应,与电池的负极连接的为阴极,发生了还原反应,由图可以知道FD为阳极,发生了氧化反应,故B选项错误;电解精炼铜时,粗铜作为电解池的阳极,F极是阳极,所以C正确;A池用石墨电极电解氢氧化钠溶液,D极产生的气体为氧气,所以该过程产生的电子数为2.24/22.4×4=0.4mol,所以B池中E极增加的质量=0.4/2×64=12.8g,故D错误。
点评:本题考查了电解池的知识,该考查是高考考查的重点和难点,本题有一定的综合性,有一定的难度。
本题难度:一般
4、选择题 用石墨做电极,电解下列溶液,经过一段时间,溶液的pH下降的是
[? ]
A.NaCl
B.NaOH
C.H2SO4
D.CuSO4
参考答案:CD
本题解析:
本题难度:一般
5、选择题 右图,是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列判断正确的是( )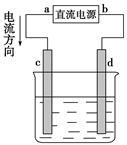
A.a为负极、b为正极
B.a为阳极、b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
参考答案:C
本题解析:有图可以看出,电流方向由a流向c,所以a为正极,b为负极,c为阳极,d为阴极,所以AB都错误,在电解过程中,d电极生成了氢氧根离子,与溶液中的铜离子生成了氢氧化铜沉淀,所以C正确;D错误,因为氯离子在a极放电,生成了氯气,所以其浓度不断变小。
点评:本题考查了电解池的基础知识,该题难度适中。该题要注意电解池电极的判断。
本题难度:简单