时间:2017-03-02 22:50:17
1、选择题 25℃时,CaCO3在水中的溶解平衡曲线如图所示.已知25℃时,CaCO3的Ksp=2.8×10-9.据图分析,下列说法不正确的是( )
A.x的数值为2×10-5
B.c点时有碳酸钙沉淀生成
C.b点与d点对应的溶度积相等
D.加入蒸馏水可使溶液由d点变到a点
参考答案:A.在d点c(CO32-)=1.4×10-4mol?L-1,因室温时,CaCO3的溶度积Ksp=2.8×10-9,所以c(Ca2+)=2×10-5mol?L-1,故x的数值为2×10-5,故A正确;
B.在c点c(Ca2+)>×10-5mol?L-1,即相当于增大c(Ca2+),平衡左移,有CaCO3生成,故B正确;
C.b点与d点在相同的温度下,溶度积相等,故C正确;
D.d点为饱和溶液,加入蒸馏水后如仍为饱和溶液,则c(Ca2+)、c(CO32-)都不变,如为不饱和溶液,则二者浓度都减小,故不可能使溶液由d点变成a点,故D错误.
故选:D.
本题解析:
本题难度:简单
2、选择题 常温下,Ksp(CaS04)=9×l0-6,常温下CaS04在水中的沉淀溶解平衡曲线如图.下列说法正确的是( )
A.常温下CaS04饱和溶液中,c(Ca2+)、c(SO42-)对应曲线上任意一点
B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×l0-3mol/L
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
参考答案:A、常温下CaS04饱和溶液中,c(Ca2+)?c(SO42-)=Ksp,Ksp(CaS04)=9×l0-6,c(Ca2+)=c(SO42-)=3×l0-3,故A错误;
B、根据图示数据,可以看出b点Qc=2×l0-5>Ksp,所以会生成沉淀,平衡向生成沉淀的方向进行,此时溶液中c(SO4-)会小于4×l0-3mol/L,故B错误;
C、升高温度,有利于溶解平衡正向移动,所以硫酸根的浓度会增大,故C错误;
D、a、c点均是常温下CaS04在水中的沉淀溶解平衡曲线上的点,所以a点对应的Ksp等于c点对应的Ksp,故D正确.
故选D.
本题解析:
本题难度:简单
3、选择题 已知25℃时,AgC1、AgBr、Agl的Ksp分别为1.8×l0-l0、5.O×10—13、8.3×10—17,用AgNO3标准溶液滴定卤素离子的过程,以滴入AgNO3溶液的体积为横坐标,pX为纵坐标:[pX= -lgc(X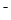 )],就可绘得滴定曲线。现以0.1 mol·L-l AgNO3溶液分别滴定20.00 mL 0.1 mol·L-lCl
)],就可绘得滴定曲线。现以0.1 mol·L-l AgNO3溶液分别滴定20.00 mL 0.1 mol·L-lCl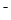 、Br
、Br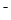 、I
、I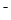 绘得滴定曲线如图,下列有关说法中正确的是
绘得滴定曲线如图,下列有关说法中正确的是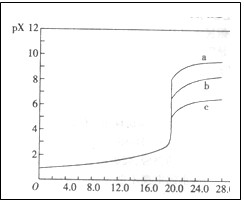
A.a、b、c分别表示Cl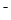 、Br
、Br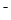 、I
、I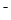
B.a、b、c分别表示I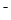 、Br
、Br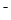 、Cl
、Cl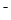
C.a、b、c分别表示Br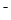 、I
、I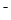 、Cl
、Cl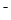
D.用硝酸银滴定法测定试样中c(Cl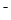 ),可用KI作指示剂
),可用KI作指示剂
参考答案:B
本题解析:pX= -lgc(X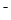 )越大,即c(X
)越大,即c(X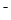 )越小,由25℃时,AgC1、AgBr、Agl的Ksp大小可得a、b、c分别表示I
)越小,由25℃时,AgC1、AgBr、Agl的Ksp大小可得a、b、c分别表示I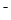 、Br
、Br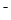 、Cl
、Cl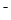 ;
;
本题难度:一般
4、填空题 (12分)按要求回答下列问题:
(1)常温下,向VL 0.1mol/L的醋酸溶液中加水稀释,下列说法中正确的是 (填字母)
A.溶液中导电粒子的数目将减少
B.由水电离的c(H+)浓度将减小
C.溶液中不变
D.溶液中 将减小
将减小
E.醋酸的电离程度将增大,c(H+)也增大
(2)①常温下,将0.1mol/L的硫酸V1mL与0.1mol/LNaOH溶液V2mL混合后,溶液的pH=1则V1:V2= (忽略溶液体积的变化)。
②常温下,若溶液由pH=3的盐酸V1mL与pH=11的某碱BOH溶液V2mL混合而得,则下列假设和结论都正确的是 (填字母)
A.若混合后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol/L
B.若V1=V2,则混合后溶液的pH一定等于7
C.若V1=V2,则混合后一定有:c(Cl-)>c(B+)>c(H+)>c(OH-)
D.混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c(OH-)
(3)常温下,浓度均为0.1mol/L的五种溶液的pH如下表所示:
| 溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
参考答案:(12分)
(1)CD (2分) (2)①2:1(1分) ②AD (2分)
(3)①ClO-+CO2+H2O==HClO+HCO3- (2分) ②A (1分) ③1.98×10-6mol/L (2分)
(4)1/3×10-8mol/L或3.3×10-9mol/L (2分)
本题解析:(1)A、向醋酸溶液中加水稀释,则醋酸的电离平衡正向移动,所以醋酸根离子、氢离子的物质的量增大,导电粒子的数目增多,错误;B、电离平衡尽管正向移动,但最终氢离子的浓度减小,则对水的抑制作用减小,所以水电离氢离子浓度增大,错误;C、溶液中 =Ka/Kw,二者都是平衡常数,温度不变,则该常数不变,正确;D、醋酸稀释后醋酸根离子浓度减小,氢离子浓度也减小,但水的电离程度增大,所以氢离子浓度减小的程度较小,所以
=Ka/Kw,二者都是平衡常数,温度不变,则该常数不变,正确;D、醋酸稀释后醋酸根离子浓度减小,氢离子浓度也减小,但水的电离程度增大,所以氢离子浓度减小的程度较小,所以 减小,正确;E、稀释时,醋酸的电离平衡正向移动,醋酸的电离度增大,但氢离子浓度减小,错误,答案选CD;
减小,正确;E、稀释时,醋酸的电离平衡正向移动,醋酸的电离度增大,但氢离子浓度减小,错误,答案选CD;
(2)①硫酸与氢氧化钠混合后的pH=1,则氢离子浓度为0.1mol/L,所以(0.1mol/L×V1mL×2-0.1mol/L×V2mL)/(V1+V2)mL=0.1mol/L,解得V1=2V2,所以V1:V2=2:1;
②A、若混合后的溶液呈中性,则c(H+)=c(OH-)=1×10-7mol/L,所以c(H+)+c(OH-)=2×10-7mol/L,正确;B、因为BOH的碱性强弱未知,所以V1=V2时,溶液可能是中性,也可能是酸性,错误;C、若V1=V2,则混合后不一定有:c(Cl-)>c(B+)>c(H+)>c(OH-),如BOH为强碱,则有若V1=V2,则混合后一定有:c(Cl-)=c(B+)>c(H+)=c(OH-),错误;D、混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c(OH-),符合电荷守恒定律,正确,答案选AD;
(3)①根据表中数据可知NaClO的碱性比碳酸钠溶液的碱性弱,则少量二氧化碳通入NaClO溶液中,只能生成碳酸氢钠和HClO,不能生成碳酸钠,则离子方程式是ClO-+CO2+H2O==HClO+HCO3-;
②将酸溶液稀释相同的倍数时,酸越弱,则加水稀释时电离度增大的程度越大,则pH增大的程度越小,四种酸中NaCN的碱性最强,说明HCN的酸性最弱,所以稀释相同倍数时pH变化最小的是HCN,答案选A;
③常温下,等浓度的醋酸与醋酸钠组成的混合溶液pH=6,则c(H+)=10-6mol/L,c(OH-)=10-8mol/L,根据电荷守恒,有c(Na+)+c(H+)=c(CH3COO-)+c(OH-),根据物料守恒,有2c(Na+)= c(CH3COO-)+c(CH3COOH),两式结合得c(CH3COO-)-c(CH3COOH)= 2c(H+)-2c(OH-)=1.98×10-6mol/L;
(4)Ksp(AgCl)=1.0×10-10= c(Cl-) c(Ag+),Ksp (CH3COOAg)=9.0×10-4= c(CH3COO-)c(Ag+),常温下,CH3COOAg若要在NaCl溶液中开始转化为AgCl沉淀,则CH3COOAg加入到氯化钠溶液中,形成饱和溶液时,银离子的浓度为3.0×10-2mol/L,若产生AgCl沉淀,则c(Cl-) c(Ag+)>1.0×10-10,c(Cl-)>1.0×10-10/ c(Ag+)=1/3×10-8mol/L。
考点:考查溶液中化学平衡的移动判断,溶度积常数的应用
本题难度:困难
5、选择题 难溶电解质AB2饱和溶液中,c(A2+)=xmol·L-1,c(B-)=ymol·L-1,则Ksp值为
[? ]
A.1/2 xy2
B.xy
C.xy2
D.4xy2
参考答案:C
本题解析:
本题难度:一般