时间:2017-03-02 22:25:49
1、选择题 常温下0.1mol・L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是?
[? ]
A.将溶液稀释到原体积的10倍?
B.加入适量的醋酸钠固体
C.加入等体积0.2?mol・L-1盐酸?
D.适当提高溶液的温度
2、选择题 下列叙述中,不正确的是( )
A.0.1?mol?L-1CH3COOH溶液加水稀释,n(H+)增大
B.0.2?mol?L-1盐酸与等体积0.05?mol?L-1Ba(OH)2溶液混合后,溶液pH为1
C.向AgCl悬浊液中滴入KI溶液,生成AgI沉淀,说明AgCl的溶解度大于AgI
D.若NH4HCO3溶液、NH4HSO4溶液和NH4NO3溶液中c(NH4+)相等,则c(NH4HSO4)<c(NH4NO3)<c(NH4HCO3)
3、选择题 已知25℃时,电离常数Ka(HF)=3.6×10-4 ,溶度积常数Ksp(CaF2) =1. 46×10 -10。现向1L 0.2mol・L-1 HF溶液中加入1L0.2mol・L-1 CaCl2溶液,则下列说法中正确的是
[? ]
A.25℃时,0.1mol・L-1HF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中有CaF2沉淀产生
D.该体系中,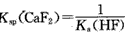
4、选择题 下列叙述正确的是( )
A.0.1?mol?L-1醋酸溶液中:c(H+)=c(CH3COO-?)+c(OH-?)
B.中和pH与体积都相同的硫酸和醋酸,消耗NaOH的量后者大于前者
C.同温度同浓度的NaOH和澄清石灰水中,水的电离程度相同
D.NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(OH-)>c(H+)
5、选择题 已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:
NaCN+HNO2 HCN+NaNO2?NaCN+HF
HCN+NaNO2?NaCN+HF HCN+NaF? NaNO2+HF
HCN+NaF? NaNO2+HF HNO2+NaF
HNO2+NaF
由此可判断下列叙述不正确的是
A.K(HF)=7.2×10-4
B.K(HNO2)=4.9×10-10
C.根据两个反应即可得出结论
D.K(HCN)<K(HNO2)<K(HF)