时间:2017-02-07 14:49:56
1、选择题 如图,隔板K可左右移动,甲中充入2 mol A和1 mol B,乙中充入2 mol C和1 mol He,此时K停在0处。发生反应2A(g)+B(g) 2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是
2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是
A.达平衡后,隔板K最终停留在左侧刻度0~2之间
B.若平衡时K停留在左侧1处,则活塞停留在右侧6处
C.达到平衡时,甲容器中B的物质的量小于于乙容器中B的物质的量
D.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
2、填空题 (12分).现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,混合体系中C的质量分数减小;当减小压强时,A的转化率变大,则:
pC(g),达到平衡后,当升高温度时,混合体系中C的质量分数减小;当减小压强时,A的转化率变大,则:
(1)该反应的逆反应为__________热反应,且m+n________p(填“>”、“=”或“<”)。
(2)加压时,B的质量分数________(填“增大”、“减小”或“不变”,下同)。B的转化率________
(3) 若C是有色物质,A、B均无色,则加入A(体积不变)时混合物颜色________;而保持容器体积不变,充入氖气时,混合物颜色________(填“变深”、“变浅”或“不变”)。
3、选择题 工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)  Si(s)+4HCl(g)?
Si(s)+4HCl(g)?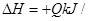 mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L・min)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应
4、选择题 在一定温度下,固定体积的密闭容器内,反应2HI(g)  ?H2(g) + I2(g)达到平衡状态的标志是:① I2的体积分数不再变化;② 生成1 mol H2同时消耗1 mol I2;③ 容器内压强不再变化;④ 生成2 mol HI同时消耗1 mol H2;⑤ 气体的密度不再变化;⑥ 混合气体的平均式量不再变化(????)
?H2(g) + I2(g)达到平衡状态的标志是:① I2的体积分数不再变化;② 生成1 mol H2同时消耗1 mol I2;③ 容器内压强不再变化;④ 生成2 mol HI同时消耗1 mol H2;⑤ 气体的密度不再变化;⑥ 混合气体的平均式量不再变化(????)
A.①②③④⑤⑥
B.①②③⑤⑥
C.①②⑤⑥
D.①②
5、填空题 (10分)高温下,炼铁高炉中存在下列平衡:FeO(s)+CO(g) 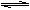 Fe(s)+CO2(g)?△H>0
Fe(s)+CO2(g)?△H>0
试回答下列问题:
⑴铁在元素周期表中位于???? ▲??? 周期??? ▲??族。
⑵写出该反应的平衡常数表达式: ▲ ,升高温度,该反应的平衡常数K值将??????
?? ▲?(填“增大”、“减小”或“不变”,下同),平衡体系中固体的质量将????▲??。
⑶为减少高炉冶铁时,含有CO的尾气排放,下列研究方向不可取的是????? ▲?????。
A.其它条件不变,增加高炉的高度
B.调节还原时的炉温
C.增加原料中焦炭与赤铁矿的比例
D.将生成的铁水 及时移出
及时移出
⑷1100℃时, FeO(s)+CO(g)  ?Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2g的FeO,同时通入4.48L的CO气体(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为 ▲???。(精确到0.1%)
?Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2g的FeO,同时通入4.48L的CO气体(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为 ▲???。(精确到0.1%)