时间:2017-02-02 07:13:57
1、填空题 选择适宜的材料和试剂设计一个原电池,完成下列反应:
Zn+CuSO4=ZnSO4+Cu
(1)画出装置图:______
(2)电极材料和电解质溶液各是什么?______
(3)写出电极反应式:
正极:______;负极:______.
参考答案:(1)根据自发的氧化还原反应:金属锌失电子,为负极,正极可以
本题解析:
本题难度:一般
2、选择题 下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+ AsO33-+I2+H2O ”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。
AsO33-+I2+H2O ”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。 
下列叙述中正确的是 [???? ]
A.甲组操作时,微安表(G)指针发生偏转
B.甲组操作时,溶液颜色变深
C.乙组操作时,C2做正极
D.乙组操作时,C1上发生的电极反应为I2 +2e-=2I-
参考答案:BD
本题解析:
本题难度:一般
3、选择题 在理论上不能用于设计原电池的化学反应是???????????????????????????(????)
A.HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)
B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)
C.2FeCl2+Cl2=2FeCl 3
3
D.3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O
参考答案:A
本题解析:略
本题难度:简单
4、选择题 如图所示,其中甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O.下列说法正确的是( )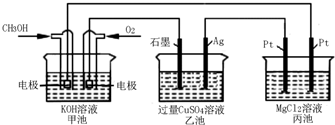
A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B.甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O=CO32-+8H+
C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D.甲池中消耗280?mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
参考答案:A、甲池是燃料电池,是化学能能转化为电能的装置,乙、丙池是电
本题解析:
本题难度:一般
5、选择题 关于如图所示装置的叙述,正确的是( )
A.锌是正极,逐渐溶解
B.硫酸根物质的量不断减小
C.阳离子向正极移动
D.电子从铜片经导线流向锌片
参考答案:C
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,失去电子;铜是正极,溶液中的氢离子得到电子,所以正确的答案选C。
本题难度:一般