时间:2017-01-24 20:05:14
1、选择题 下列实验操作或事实与预期实验目的或所得结论一致的是(??? )
参考答案:D
本题解析:A 错 可能含有碳酸氢根离子,亚硫酸根离子、亚硫酸氢根离子
B 错 硅酸的酸性比碳酸强
C?错KI会被空气中的氧气氧化,生成单质碘,从而显黄色。
D 对常温下,铁在浓硝酸中钝化
本题难度:一般
2、实验题 如图所示是在实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出。
(1)在组装好装置后,若要检验A—E装置的气密性,其操作是首先???????,然后微热A,???察到E中有气泡冒出,移开酒精灯或松开双手,E中导管有水柱形成说明装置气密性良好。
(2)装置B中盛放试剂是???????????????。
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹1,从分液漏斗放出浓氨水至浸没烧瓶中固体后关闭分液漏斗,稍后片刻,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时产生????????(答现象);从E中逸出液面的气体可以直接排入空气,请写出在C中发生反应的化学方程式??????????。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量。若反应前固体质量为16g,反应后称重固体质量减少2.4g。通过计算确定该固体产物的成分是??????????(用化学式表示)。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸流入F中。写出产生白烟的化学方程式 ?????????????。迅速产生倒吸的原因是??????????。
参考答案:(1)首先关闭弹簧夹2和分液漏斗活塞,打开弹簧夹1
(
本题解析:(1)组装好装置后,若要检验A-E装置的气密性,其操作是:首先关闭弹簧夹2和分液漏斗活塞,打开弹簧夹1,在E中装入水后,然后微热A,观察到E中有气泡冒出,移开酒精灯或松开双手,E中导管有水柱形成说明装置气密性良好。
(2)进入C中硬质试管的氨气应干燥,装置B的作用是干燥氨气,干燥氨气用碱石灰。
(3)反应后的尾气中含有未反应的氨气,氨气在E溶液中与二氧化硫反应生成亚硫酸铵,亚硫酸铵与氯化钡反应生成亚硫酸钡,故还有白色沉淀沉淀,装置C中黑色固体逐渐变红,说明有Cu生成,从E中逸出液面的气体可以直接排入空气,说明氨气被氧化为氮气,同时生成水,C中发生反应的化学方程式为:2NH3+CuO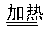 Cu+N2↑+H2O
Cu+N2↑+H2O
(4)16gCuO中含有Cu元素质量为16g×62/80==12.8g,含有氧元素质量为16g-12.8g=3.2g,反应后称重固体质量减少2.4g,剩余固体质量为16g-2.4g=13.6g,大于12.8g,故剩余固体含有Cu、O元素,故n(Cu)=12.8g÷64g/mol=0.2mol,含有O元素的质量为13.6g-12.8g=0.8g,n(O)=0.8g÷16g/mol
=0.05mol,n(Cu):n(O)=0.2mol:0.05mol=4:1>2:1,故剩余固体为Cu2O、Cu。
(5)氯气有强氧化性,氧化氨气生成N2,产生白烟,说明生成固体,故还生成NH4Cl,反应方程式为:3Cl2+8NH3=N2+6NH4Cl.盛满氯气的集气瓶中因氨气消耗氯气生成部分固体,导致内压减小,引起溶液倒吸。
本题难度:困难
3、选择题 下列实验不能达到预期目的的是
A.利用Ⅰ制取Fe(OH)2
B.利用Ⅱ装置制取C2H4
C.利用Ⅲ装置进行铜与浓硝酸反应的实验
D.利用Ⅳ装置收集NH3
参考答案:B
本题解析:A:可防止Fe(OH)2被空气氧化,正确
B:温度计应插入混合液中,控制混合液温度,不正确
C:可随时控制反应的发生与停止,并且可防止污染空气,正确
D:氨气密度小于空气,应从短管进集气瓶,并且极易溶于水,用倒置的漏斗防止倒吸,正确
本题难度:一般
4、简答题 (10分)活性氧化锌用途非常广泛。以氧化锌粗品(含铁的氧化物、CuO和SiO2等杂质)为原料制备活性氧化锌并生产其它副产品的生产工艺流程如下:
已知:Zn(OH)2可溶于NaOH溶液。
请回答下列问题:
(1)“溶解”前将氧化锌粗品粉碎成细颗粒,其目的是????????。
(2)操作A所得滤渣的主要成分是??????。
(3)加入过量Fe时,滤液M中与Fe反应的离子有???????。
(4) 操作C所得的滤渣P中含有Fe(OH)2和Fe(OH)3,请写出生成Fe(OH)3的化学反应方程式为?????。
(5)“沉淀”的成分为ZnCO3·2Zn(OH)2·H2O,可用氧化物的形式把它改写为????????。
参考答案:(1)增大接触面积使其能充分反应(2分)(2)SiO2(2分
本题解析:
试题分析:根据题给信息和化学工艺流程知,氧化锌粗品(含铁的氧化物、CuO和SiO2等杂质)在稀硫酸中溶解生成硫酸铜、硫酸锌、硫酸铁和硫酸亚铁,经操作A过滤,滤渣的成分为二氧化硅;向滤液M中加入过量铁,铁与硫酸铁反应生成硫酸亚铁,铁与硫酸铜反应生成硫酸亚铁和铜,过滤得滤渣铁和铜的混合物,滤液N为硫酸亚铁和硫酸锌的混合物;向滤液N中加过量氢氧化钠溶液,铁元素转化为氢氧化物沉淀,过滤,滤渣P含有Fe(OH)2和Fe(OH)3,滤液Q酸化后加入碳酸钠溶液,锌元素转化为沉淀,煅烧得氧化锌。(1)“溶解”前将氧化锌粗品粉碎成细颗粒,其目的是增大接触面积使其能充分反应;(2)由上述分析知,操作A所得滤渣的主要成分是SiO2;(3)加入过量Fe时,滤液M中与Fe反应的离子有H+、Cu2+、Fe3+;(4)Fe(OH)2与氧气、水反应生成Fe(OH)3的化学反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3; (5)“沉淀”的成分为ZnCO3·2Zn(OH)2·H2O,可用氧化物的形式把它改写为3ZnO·CO2·3H2O。2等杂质)为原料制备活性氧化锌并生产其它副产品的生产工艺流程为载体考查物质的分离提纯、化学方程式的书写及阅读材料接受信息的能力。
本题难度:一般
5、实验题 (共22分)某实验小组用下列装置进行如下的实验。?
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
????????????????????????????????、??????????????????????????????????。
实验小组在不断鼓入空气的情况下,熄灭酒精灯,发现反应仍能继续进行,说明该反应是?? ?? ?反应。
(2)甲和乙两个水浴作用不相同。甲的作用是??????????????????????????????;
乙的作用是?????????????????????????????。
(3)反应进行一段时间后,干燥的試管a中能收集到不同的物质,那么收集到的有机物是(请填写其结构简式)?????????;集气瓶中收集到的气体的最主要成分是?????。(填写气体的分子式)
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,实验小组的同学认为这可能是存在副产物乙酸。除去该物质,可以使用厨房中常见的一种化合物,该物质为???? 。(填写化学式或分子式)
。(填写化学式或分子式)
(5)请写出以上实验涉及的有机物乙醇在生活生产中的一种具体应用:????????????。
(6)该实验的目的是:?????????????????????????????????????
参考答案:(1)(6分)2Cu+O2本题解析:考查乙醇催化氧化原理
(1)红色是铜的颜色,黑色是氧化铜的颜色。说明在加热的条件下铜被空气氧化生成氧化铜,氧化铜在加热的条件下又被乙醇还原生成了铜。熄灭酒精灯后,反应仍然能进行,说明反应是放热反应,放出的热量足以维持反应的进行。
(2)根据装置可判断,进入玻璃管的是乙醇气体,所以通过加热使乙醇挥发,产生乙醇气体。而要得到生成物乙醛,就必须降低温度,使乙醛液化变成液体,便于收集。
(3)反应连续进行的,即部分乙醇来不及被氧化,和生成的乙醛一同进入小试管中。而空气中的氮气难溶于水,且不参与反应,被收集到集气瓶中。
(4)试纸显红色,说明溶液显酸性,这说明在反应过程中有乙酸生成,所以要除去乙酸,可以用碳酸氢钠或碳酸钠溶液即可。
(5)75%的酒精溶液,常原来作消毒剂。
(6)根据实验原理及装置可知实验目的是来探究乙醇催化氧化实验的。
本题难度:一般