时间:2017-01-24 19:06:45
1、选择题 某固体仅由一种元素组成,其密度为5.0g・cm-3。用X射线研究该固体的结构得知:在边长为10-7cm的正 方体中含有20个原子。则此元素的相对原子质量最接近于下列数据中的 [???? ]
A.32
B.120
C.150
D.180
2、选择题 下列各组物质汽化或熔化,所克服的微粒间的作用力,属于同种类型的是?
A.碘单质的升华和金刚石的熔化
B.二氧化硅和氯化钾的熔化
C.氧化铝和冰的熔化
D.乙醇和液氯的汽化
3、选择题 下列关于晶体的说法一定正确的是(???)
A.分子晶体中都存在共价键
B.CaTiO3晶体中每个Ti4+和12个O2-相紧邻
C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.熔融时化学键没有破坏的晶体一定是金属晶体
4、填空题 已知A、B、C、D、E五种元素的性质或结构信息如下,请根据信息回答下列问题:
(1)已知短周期元素A、B原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 ①某同学根据上述信息,推断B的核外电子排布如图所示,该同学所画的电子排布图违背了______。 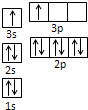 ②ACl2分子中A的杂化类型为__________,ACl2空间构型为__________。 (2)已知C单质曾被称为“银色的金子”,与锂形成的合金常用于航天飞行器,其单质能溶于强酸和强碱。D是周期表中电负性最大的元素。E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物。请根据上述信息。 ①写出E元素原子基态时的电子排布式____________________。 ②以C单质、镁、NaOH溶液可以构成原电池,则负极的电极反应式为__________。 ③D与Ca2+可形成离子化合物,其晶胞结构如图所示。其中Ca2+离子的配位数为__________,若该晶体的密度为ag/cm3,则该晶胞的体积是__________cm3(写出表达式即可)。 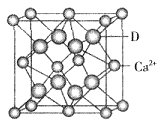 5、选择题 下列说法正确的是( ) |