时间:2017-01-24 19:04:27
1、选择题 下列说法中不正确的是
A.与煤油、柴油相比较,天然气是一种比较清洁的化石燃料
B.乙醇是一种可再生能源,作为燃料的优点的是完全燃烧的产物不污染环境
C.利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量
D.煤的气化和液化不仅可以获得洁净燃料,而且再燃烧会放出更多的热量
2、选择题 已知25℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol・L-1 HF溶液中加入1 L 0.2 mol・L-1 CaCl2溶液,则下列说法中,正确的是
A.HF与CaCl2反应产生沉淀
B.25℃时0.2mol・L-1HF溶液中pH=2
C.Ksp(CaF2)随温度和浓度的变化而变化
D.该体系中最终没有氟化氢分子
3、实验题 (8分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol・ L-1盐酸、0.55mol・ L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ 已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ・℃-1・ Kg-1,各物质的密度均为1g・cm-3。 计算完成上表。△H= (3)某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题: 研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃,此反应所用NaOH溶液的浓度应为 mol/L。 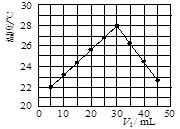 4、选择题 室温时,向10mL的醋酸稀溶液中逐滴滴入NaOH稀溶液至过量,有关叙述正确的是 5、选择题 下列说法不正确的是 | |