时间:2017-01-19 09:55:17
1、选择题 将适量铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe2+和Fe3+溶度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是
A.2 :3
B.3 :2
C.1 :2
D.1 :1
2、选择题 下列化合物不是黑色的是
A.FeO
B.FeS
C.Fe3O4
D.Fe2O3
3、选择题 向含有FeCl3和BaCl2的酸性溶液中通入足量的SO2,有白色沉淀生成,过滤后向滤液中滴入KSCN溶液时,无明显现象,由此得出的正确结论是(???)
A.白色沉淀是BaSO3
B.白色沉淀是BaSO4
C.白色沉淀是BaSO3和BaSO4的混合物
D.FeCl3已全部被SO2还原成FeCl2
4、简答题 (15 分)废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧电池的铜帽(Cu、Zn 总含量约为99%)回收Cu并制备ZnO 的部分实验过程如下: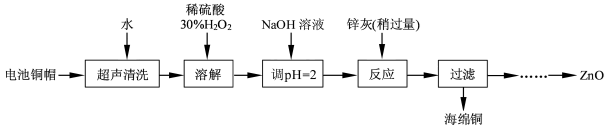
(1)①铜帽溶解时加入H2O2的目的是???????????????????????????????????(用化学方程式表示)。②铜帽溶解完全后, 需将溶液中过量的H2O2除去。除去H2O2的简便方法是????????????????。
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中反应的离子方程式如下:摇摇2Cu2++4I-=2CuI(白色)↓+I2???? 2S2O32- +I2=2I-+S4O62-
①滴定选用的指示剂为???????????????,滴定终点观察到的现象为??????????????????????。
②若滴定前溶液中的H2O2没有除尽,所测定的Cu2+含量将会???(填“偏高”、“偏低”或“不变”)。
(3)已知pH>11 时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1. 0 mol·L-1计算)。
| ? | 开始沉淀的pH | 沉淀完全的pH | ||||
| Fe3+ | 1. 1 | 3. 2 | ||||
| Fe2+ | 5. 8 | 8. 8 | ||||
| Zn2+ | 5. 9 | 8. 9 实验中可选用的试剂:30%H2O2、1. 0 mol·L-1HNO3、1. 0 mol·L-1NaOH。由除去铜的滤液制备ZnO 的实验步骤依次为:①??????;②???????;③过滤;④??????????;⑤过滤、洗涤、干燥;⑥900℃煅烧。 5、简答题 利用染化厂的废料铁泥(主要成分是Fe2O2、FeO和铁)制备可用于隐形飞机涂层的纳米四氧化三铁的生产流程为:
|