时间:2017-01-19 01:40:10
1、选择题 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),pc(CO32-)=-lgc(CO32-).下列说法正确的是( )
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO32-)
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-)
D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32-)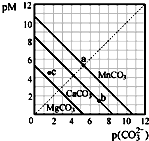
2、填空题 炼锌厂产生的工业废渣――锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4・7H2O和金属镉(Cd)是一个有益的尝试,其流程如下:
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7。试回答下列问题:
(1)浸出时用到的试剂X为 , 写出溶解过程中加快浸出速率和提高浸出率的两点措施:_______________________________,______________________________。
(2)写出加入Ca(ClO)2反应的离子方程式 。
(3)调节pH过程可以选用 (填“ZnO”或“NaOH”);本流程的pH调节一般调至5,其目的是 。
(4)写出过滤后加入过量的锌粉反应的离子方程式 。
(5)在蒸发浓缩操作时,要采取实验措施是: 。
3、简答题 镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害.某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+.
②已知实验温度时的溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O
③某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如下表所示:
| M(OH)n | Ksp | pH 开始沉淀 沉淀完全 Al(OH)3 1.9×10-23 3.4 4.2 Fe(OH)3 3.8×10-38 2.5 2.9 Ni(OH)2 1.6×10-14 7.6 9.8 回答下列问题: (1)用NiO调节溶液的pH,依次析出沉淀Ⅰ______和沉淀Ⅱ______(填化学式). (2)写出加入Na2C2O4溶液的反应的化学方程式:______. (3)检验电解滤液时阳极产生的气体的方法:______. (4)写出“氧化”反应的离子方程式:______. (5)如何检验Ni(OH)3已洗涤干净?______. 4、填空题 镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下: 5、选择题 有关AgCl沉淀的溶解平衡说法正确的是 [???? ] |