时间:2017-01-18 23:41:26
1、填空题 工业生产无铁硫酸铝,以硫酸浸取铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)得含铁(Fe3+)的硫酸铝溶液,加热到一定温度,搅拌,加入一定量高锰酸钾溶液和硫酸锰溶液,在溶液中生成活性二氧化锰,调节溶液的pH,反应一段时间,二氧化锰和Fe?(OH)?3发生吸附共沉作用,最终得到无铁硫酸铝产品.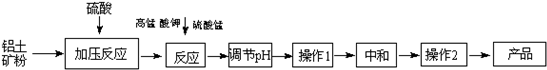
(1)硫酸浸取铝土矿时主要反应的离子方程式为______;
(2)完成高锰酸钾溶液和硫酸锰溶液反应的化学方程式:2KMnO4+3MnSO4+2H2O=______;
(3)调节pH的作用是______;
(4)操作1的名称为______,实验室进行操作2用到的陶瓷质仪器有______;
(5)下列有关工艺的说法正确的是______(双选,填字母).
A.可以向溶液中再加入铝土矿粉等调节pH
B.溶液的碱性越强,则除铁效果越好,而且不会影响硫酸铝的产率
C.活性二氧化锰生成量应适宜,不足时铁的去除率较低,过量时会增加成本
D.可以直接向溶液中加入二氧化锰粉末以除去Fe?(OH)?3.
参考答案:(1)铝土矿的主要成分是Al2O3,加入硫酸主要发生:Al2
本题解析:
本题难度:一般
2、选择题 38.4 g铜跟适量的浓硝酸反应,铜全部作用后,共收集到22.4L(标准状况,不考虑N2O4)气体。则反应消耗HN03的物质的量可能是
A.1 mol
B.1.6 mol
C.2.2 mol
D.2.4 mol
参考答案:C
本题解析:铜和硝酸反应时,硝酸表现酸性和氧化性,故通过铜的物质的量可求出成盐的硝酸的物质的量是1.2 mol,根据22.4 L气体可求出被还原的硝酸的物质的量是1 mol(N原子守恒),则共消耗的HNO3的物质的量是2.2 mol。
本题难度:简单
3、填空题 Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu。现有浓硫酸、浓硝 酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸,简述如何用简便的实验方法来检验CuO经
酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸,简述如何用简便的实验方法来检验CuO经 氢气还原所得红色产物中是否含有碱性氧化物Cu2O。
氢气还原所得红色产物中是否含有碱性氧化物Cu2O。
参考答案:取少量待检样品放入稀硫酸,振荡,若溶液变为蓝色,说明样品中有
本题解析: 由题给信息可知,Cu2O是碱性氧化物,可溶于酸溶液:Cu2O+2H+=2Cu++H2O;而Cu+在酸溶液中不稳定,自身歧化成Cu2+和Cu。2Cu+=Cu2++Cu。题给试剂中,浓硫酸、浓硝酸、稀硝酸、FeCl3稀溶液均显酸性,且都能与Cu反应生成Cu2+,如果选用这些试剂,它们和样品反应后的溶液都呈蓝色(Cu
由题给信息可知,Cu2O是碱性氧化物,可溶于酸溶液:Cu2O+2H+=2Cu++H2O;而Cu+在酸溶液中不稳定,自身歧化成Cu2+和Cu。2Cu+=Cu2++Cu。题给试剂中,浓硫酸、浓硝酸、稀硝酸、FeCl3稀溶液均显酸性,且都能与Cu反应生成Cu2+,如果选用这些试剂,它们和样品反应后的溶液都呈蓝色(Cu
本题难度:一般
4、简答题 在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4制备Fe(OH)2白色沉淀.
①在试管Ⅰ里加入的试剂是______.
②在试管Ⅱ里加入的试剂是______.
③为了制得Fe(OH)2白色沉淀,正确的操作顺序是______(填下列序号)
A.打开止水夹????????B.检验试管Ⅱ出口处排出的H2的纯度
C.夹紧止水夹????????D.在试管Ⅰ和Ⅱ中加入试剂,塞紧塞子
④写出此过程中涉及到的化学方程式______.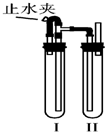
参考答案:①铁与硫酸反应生成氢气,关闭止水夹,会使装置Ι中压强变大,使
本题解析:
本题难度:一般
5、填空题 (本题6分)
⑴电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
①检验溶液中Fe3+存在的试剂是????????? __,证明Fe3+存在的现象是????????? __。]②写出FeCl3溶液与金属铜发生反应的化学方程式:??????????????????????????。
⑵ 3Cl2??+ 6NaOH? ="=?" 5NaCl + NaClO3?+ 3H2O
氧化剂与还原剂的物质的量之比为????????,氧化产物是????????? ________。
参考答案:①KSCN溶液,溶液变成血红色。
②? 2FeCl3
本题解析:略
本题难度:一般