??��??
.
?
CuSO4+SO2��+2H2O
D����CuSO4��2Cu+O2=2CuO��CuO+H2SO4��ϡ��=CuSO4+H2O
�ο��𰸣�C
���������
�����Ѷȣ���
2��ѡ���� ���л�������ԭ��������ǣ�???��
�ٿ����õ�����ڵ��Ȼ��Ƶķ�������ȡ�����Ƣڿ������Ƽ����Ȼ�þ������Һ����ȡþ���õ�ⷨ����ʱ��ԭ�����Ȼ�����������¯���������ķ�Ӧ���Ƿ��ȵģ����������
A���ڢ�
B���٢�
C���٢ڢ�
D���ڢۢ�
�ο��𰸣�D
����������ơ�þ�������ǻ��õĽ�����ұ������Ҫ��⡣����ȷ���ڲ���ȷ���Ƽ���ˮ��Ӧ��Ӧ�õ�����ڵ��Ȼ�þ���Ȼ����ǹ��ۻ��������ʱ�����磬�۲���ȷ����Ӧ�Ƿ��ȷ�Ӧ����������ζ�ŷ�Ӧ����Ҫ���ȣ��ܲ���ȷ����ѡD��
�����Ѷȣ���
3������� ��(21��)�ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����塣��ԭ��Ϊ��
N2(g)+3H2(g)  ?2NH3(g)??��H= -92.4KJ/mol??���ݴ˻ش��������⣺
?2NH3(g)??��H= -92.4KJ/mol??���ݴ˻ش��������⣺
��1�������йظ÷�Ӧ���ʵ���������ȷ���ǣ�ѡ����ţ�?????????��
a�������¶ȿ����������Ӱٷ������ӿ췴Ӧ����
b������ѹǿ�����������Ӱٷ��������Բ����Լӿ췴Ӧ����
c��ʹ�ô�������ʹ��Ӧ�Ļ�ܽ��ͣ��ӿ췴Ӧ����
d������Ӽ�����������ײΪ��Ч��ײ
e�������¶ȣ�V����V�����С��V����С�ı���С��V���С�ı�����
f��������һ��������£����������ı������С���Է�Ӧ����������Ӱ��
��2���ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=_______________________��
�ڸ����¶ȶԻ�ѧƽ��Ӱ�����֪�����ڸ÷�Ӧ���¶�Խ�ߣ���ƽ�ⳣ����ֵԽ_____ ��
��3��ij�¶��£�����10 mol N2��30 mol H2�������Ϊ10 L���ܱ������ڣ���Ӧ�ﵽƽ��״̬ʱ�����ƽ���������а����������Ϊ20%������¶��·�Ӧ��K=___________�����÷�����ʾ������˵���÷�Ӧ�ﵽ��ѧƽ��״̬����???????????????������ĸ����
a�������ڵ��ܶȱ��ֲ���??????????????
b��������ѹǿ���ֲ���????
c��������N2����2���棨NH3��????????????
d�����������c��NH3������
e.�����ڻ�������ƽ��Ħ���������ֲ���
��4�����ںϳɰ���Ӧ���ԣ������й�ͼ��һ����ȷ���ǣ�ѡ����ţ�_____________��
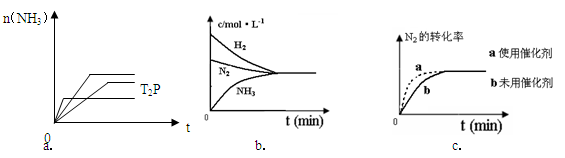
 ��5����ͬ�¶��£��к����ܱ�����A�ͺ�ѹ�ܱ�����B���������о�����1mol N2��3 molH2����ʱ�������������ȡ���һ�������·�Ӧ�ﵽƽ��״̬��A��NH3���������Ϊa���ų�����Q1 kJ��B��NH3���������Ϊb���ų�����Q2 kJ����a_____b(��>��=��<)�� Q1_____ Q2(��>��=��<)�� Q1_____92.4(��>��=��<)��
��5����ͬ�¶��£��к����ܱ�����A�ͺ�ѹ�ܱ�����B���������о�����1mol N2��3 molH2����ʱ�������������ȡ���һ�������·�Ӧ�ﵽƽ��״̬��A��NH3���������Ϊa���ų�����Q1 kJ��B��NH3���������Ϊb���ų�����Q2 kJ����a_____b(��>��=��<)�� Q1_____ Q2(��>��=��<)�� Q1_____92.4(��>��=��<)��
�ο��𰸣���1��a��c��f��e��??��4�֣�
��2����![]()
�����������1������ѹǿ������λ����ڻ���Ӱٷ���������������Ӧ���ʣ�b����ȷ������Ӽ�����������ײ��һ��������Ч��ײ�����ܹ�������ѧ�仯����ײ��Ϊ��Щ��ײ��d����ȷ���������ȷ�ģ���ѡacef��
��2����ƽ�ⳣ������һ�������£����淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ����֮���ı�ֵ�����Ա���ʽΪ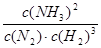 �����Ѷȣ�һ��
�����Ѷȣ�һ��
4��ѡ���� ������Ĺ�ҵ�Ʒ��У����������������Բ�ȡ�˲�������Ҫԭ�����������ȷ���ǣ���
A��������ȼ��ǰ��Ҫ���飬��Ϊ���IJ����ڿ���ȼ��
B������¯������¯���辻������Ϊ���е�SO2�������ʷ�Ӧ
C��SO2����ΪSO3ʱ��ʹ�ô��������������IJ���
D��SO3��98.3%��Ũ�������գ�Ŀ���Ƿ�ֹ�γ���������ʹSO3������ȫ
�ο��𰸣�D
���������
���������������ȼ��ǰ��Ҫ�����Ŀ��������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ�A����ȷ��B����ȷ��������ʹ�����ж���B����ȷ���������ܸı�ƽ��״̬������C����ȷ�������ȷ�Ĵ�ѡD��
�����������������Ի�ѧ��Ӧԭ��Ϊ���ݣ���ʵ�����о�Ϊ�������κ����ɵ���ɶ�Ҫ���ϻ�ѧ��Ӧ���ɡ�
�����Ѷȣ�һ��
5������� ����ѧ--ѡ��2��ѧ�뼼������15�֣�
������أ�K2FeO4����һ�ּ�������������������һ������Ͷ��ˮ���������������������£�
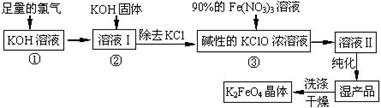
��֪��2KOH + Cl2 �T KCl + KClO + H2O���������¶Ƚϵͣ�
����? 6KOH + 3Cl2 �T 5KCl + KClO3 + 3H2O���������¶Ƚϸߣ�
�����ش��������⣺
��1�����������շ�Ӧ��Ӧ�������� ����¶Ƚϸߡ����¶Ƚϵ͡���������½��У�
��2��д����ҵ����ȡCl2�Ļ�ѧ����ʽ�������������� ����������������������
��3��K2FeO4����ǿ�����Ե�ԭ������������������������ ��
��4������KOH��Һʱ������ÿ100 mLˮ���ܽ�61.6 g KOH���壨 ����Һ���ܶ�Ϊ1.47 g/mL������
�����ʵ���Ũ��Ϊ������ ��������������������������
��5���ڡ���ҺI���м�KOH�����Ŀ������������ ������������������������
A���� ����ҺI�� �й�����Cl2������Ӧ�����ɸ����KClO
B��KOH�����ܽ�ʱ��ų��϶����������������߷�Ӧ����
C��Ϊ��һ����Ӧ�ṩ��Ӧ�����
D��ʹ������KClO3ת��Ϊ KClO
��6���ӡ���ӦҺII���з����K2FeO4�����и���Ʒ����������д��ѧʽ�������Ƕ�����Ҫ�Ļ��� ��??Ʒ������˵������һ�����ʵ���;���������������������� ����1�㼴�ɣ��� ��Ӧ���з��������ӷ�Ӧ����ʽΪ????????????????????????????????????????��
��7������ж�K2FeO4�����Ѿ�ϴ�Ӹɾ�??????????????????????????????��
�ο��𰸣���15�֣�
��1���¶Ƚϵ�?��1�֣�
��2��2N
���������
�����������1�����������շ�Ӧ��Ӧ�ڽϵ��¶��½��У���Ϊ������õ�KClO��Һ��
��2����ҵ����ȡCl2����ͨ����ⱥ��ʳ��ˮ�ķ�������ѧ����ʽΪ2NaCl + 2H2O  ��2NaOH + H2�� + Cl2����
��2NaOH + H2�� + Cl2����
��3��K2FeO4����ǿ�����Ե�ԭ����FeԪ�صĻ��ϼ���+6�ۣ��õ��ӣ�����
�����Ѷȣ�һ��