时间:2017-01-17 09:35:09
1、选择题 常温下,下列物质的水溶液,其pH小于7的是
A.Na2CO3
B.NH4NO3
C.Na2SO4
D.KNO3
2、选择题 已知0.1 mol/L的碳酸氢钠溶液的pH为8.4,则下列说法正确的是(????)
A.加入少量NaOH固体,钠离子和碳酸根离子浓度均增大
B.将该溶液加水稀释,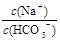 的比值保持不变
的比值保持不变
C.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
D.c(Na+)=c(HCO3-)+2c(CO32-)+c(H2CO3)
3、填空题 A、B代表不同的物质,都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两种组合。要求:相同浓度时,A1溶液中水的电离程度小于A2溶液中水的电离程度;相同浓度时,B1溶液中水的电离程度小于B2溶液中水的电离程度。请填写下列空白:
(1)写出化学式:A1___________、A2__________、B1___________、B2___________。
(2)相同温度下,当A1、B1的物质的量浓度相等时,两种溶液中水电离出的氢离子的物质的量浓度之比为________。
(3)0.1mol?L-1NaNO2溶液中离子浓度由大到小的顺序为___________________________________。
(4)B1溶液中水的电离程度小于B2溶液中水的电离程度,原因是___________。
(5)常温下,若B1、B2两种溶液的pH=5,则两溶液中由水电离出的氢离子的物质的量浓度之比为________。
4、选择题 下列离子分别加入纯水中,能使水中c(OH-)增大的是()
A.Cl-
B.ClO-
C.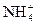
D.Na+
5、选择题 室温下,下列混合溶液中,各离子浓度的关系正确的是(?????)
A.浓度均为0.1mol・L-1的小苏打溶液与烧碱溶液等体积混合:
2c(CO32-)+c(OH-)+c(HCO3-)―c(H+)=0.1mol・L-1
B.浓度均为0.1mol・L-1的硫酸氢铵溶液与氢氧化钠溶液等体积混合
c(SO42-)>c(Na+)>c(NH4+)>c(H+)>c(OH-)
C.pH=12的氨水与pH =2的盐酸等体积混合
c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.浓度均为0.1mol・L-1的醋酸溶液与氢氧化钠溶液等体积混合
c(Na+)=c(CH3COO-)>c(OH―)=c(H+)