时间:2017-01-16 15:58:42
1、选择题 在同温同压下,关于等质量的CO2和SO2气体,下列说法不正确的是
A.CO2和SO2的分子数比为16:11
B.CO2和SO2的物质的量相同
C.CO2和SO2的体积比为16:11
D.CO2和SO2的密度比为11:16
参考答案:B
本题解析:分析:同温同压下,气体的Vm相等,根据n=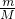 =
=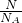 =
= 计算相关物理量.
计算相关物理量.
解答:A.N(CO2)=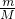 ×NA=
×NA=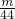 NA,N(SO2)=
NA,N(SO2)=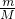 ×NA=
×NA=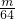 NA,二者的分子数比为64:44=16:11,故A正确;
NA,二者的分子数比为64:44=16:11,故A正确;
B.n(CO2)=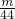 mol,n(SO2)=
mol,n(SO2)=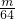 mol,二者的物质的量不同,故B错误;
mol,二者的物质的量不同,故B错误;
C.由n=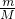 =
= 可知,同温同压下,等质量的两种气体的体积之比与摩尔质量呈反比,为64:44=16:11,故C正确;
可知,同温同压下,等质量的两种气体的体积之比与摩尔质量呈反比,为64:44=16:11,故C正确;
D.由ρ=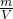 =
=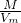 可知,二者的密度之比与摩尔质量呈正比,为44:64=11:16,故D正确.
可知,二者的密度之比与摩尔质量呈正比,为44:64=11:16,故D正确.
故选B.
点评:本题考查阿伏加德罗定律及其推论,题目难度不大,注意把握相关计算公式的推导及应用.
本题难度:一般
2、选择题 只给出下列甲和乙中对应的量,可以组成一个有关(或含有)物质的量的公式
A.①②
B.①②④
C.①②③
D.①②⑤
参考答案:B
本题解析:分析:①根据微粒数目和物质的量的关系公式n=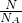 分析;
分析;
②根据标准状况下的气体体积和物质的量的关系公式n=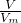 来分析;
来分析;
③根据m=ρV、n=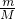 来分析;
来分析;
④依据 n=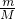 分析;
分析;
⑤、根据w=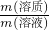 ×100%??? n=cV分析.
×100%??? n=cV分析.
解答:①由n=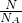 可知,利用物质的粒子数(N)、阿伏加德罗常数(NA)可以计算物质的量,故①选;
可知,利用物质的粒子数(N)、阿伏加德罗常数(NA)可以计算物质的量,故①选;
②由n=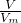 可知,利用标准状况下的气体摩尔体积(Vm)、标准状况下的气体体积(V)可以计算物质的量,故②选;
可知,利用标准状况下的气体摩尔体积(Vm)、标准状况下的气体体积(V)可以计算物质的量,故②选;
③由m=ρV,n=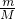 可知,利用体积、密度只能计算其质量,但摩尔质量(M)未知,则不能计算出其物质的量,故③不选;
可知,利用体积、密度只能计算其质量,但摩尔质量(M)未知,则不能计算出其物质的量,故③不选;
④依据n=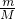 ,可以计算物质的量,故④选;
,可以计算物质的量,故④选;
⑤由n=cV可知,利用溶液中溶质的质量分数和溶液体积,不能计算溶质的物质的量,故⑤不选;
故选①②④.
故选B.
点评:本题考查以物质的量为中心的基本计算,清楚计算公式即可解答,比较基础.
本题难度:一般
3、选择题 下列叙述中,能证明某物质是弱电解质的是:
A.熔化时不导电
B.水溶液的导电能力很差
C.不是离子化合物,而是极性共价化合物
D.溶液中已电离的离子和未电离的分子共存
参考答案:D
本题解析:试题分析:在溶液中不完全电离,存在电离平衡的电解质是弱电解质,所以溶液中有已电离的离子和未电离的分子共存时,就可以说明该电解质是弱电解质,答案选D。
考点:考查弱电解质的有关判断
点评:弱电解质的证明,是基于与强电解质对比进行的。弱电解质与强电解质最大的区别就是弱电解质存在电离平衡,而强电解质不存在电离平衡。因此只要证明有电离平衡存在,就证明了弱电解质。
本题难度:简单
4、选择题 范德华力为a?KJ・mol-1,化学键为b?KJ・mol-1,氢键为c?KJ・mol-1,则a、b、c的大小关系正确的是
A.a>b>c
B.b>a>c
C.c>b>a
D.b>c>a
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列有关反应的说法不正确的是
A.在光照条件下,甲烷能与氯气发生取代反应
B.乙醛能被还原成乙酸
C.乙醇与钠单质能发生置换反应
D.乙烯能与溴发生加成反应
参考答案:B
本题解析:
本题难度:困难