时间:2017-01-16 15:48:08
1、填空题 液氨与水性质颇为相似,其电离方程式可表示为:2NH3 NH4++NH2-。某温度下其离子积常数为1×10-30(mol・L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
NH4++NH2-。某温度下其离子积常数为1×10-30(mol・L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
参考答案:(1)向正方向
(2)29
本题解析:2.3gNa加入液氨后发生反应2Na+2NH4+=2Na++2NH3+H2↑, c(NH4+)减小,平衡向正反应方向移动,2.3gNa的物质的量为0.1mol,所以生成NH2-的物质的量为0.1mol,c(NH4+)=1×10-30(mol・L-1)/ 0.1mol・L-1= 1×10-29mol・L-1,pNH4+=29
本题难度:简单
2、选择题 某温度下,水的离子积约为1×10-12,将Va L pH=2的硫酸溶液与Vb L pH=11的NaOH溶液混合,若混合溶液的pH=10,体积是(Va+Vb) L,则Va∶Vb为 (?????? )
A.2∶11
B.2∶9
C.11∶2
D.9∶2
参考答案:D
本题解析:略
本题难度:一般
3、选择题 已知:
2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2 ΔH=-226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是 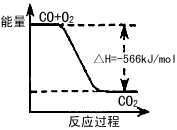 [???? ]
[???? ]
A.CO的燃烧热为283kJ
B.上图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数为6.02×1023
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列热化学方程式中,ΔH能正确表示物质的燃烧热的是( )
A.S(s)+O2(g)===SO2(g) ΔH=-269.8 kJ/mol
B.C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ/mol
C.H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ/mol
D.2C8H18(l)+25O2(g)===16CO2(g)+18H2O(l)ΔH=-11036 kJ/mol
参考答案:A
本题解析:燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以选项A正确;B中碳没有完全燃烧,C中水的稳定状态应该是液态,D中可燃物不是1mol,均是错误的,所以答案选A。
本题难度:一般
5、选择题 下列有关说法中正确的是(???)
A.HCO3―水解:HCO3―+H2O  CO32―+H3O+
CO32―+H3O+
B.中和滴定时眼睛必须注意锥形瓶内溶液颜色的变化
C.电解水生成H2和O2的实验中,可加入少量盐酸或硫酸增强导电性
D.用等浓度(0.5 mol・L-1)等体积(50 mL)的NaOH溶液与盐酸混合测定中和热
参考答案:B
本题解析:
试题分析:HCO3―+H2O  ?CO32―+H3O+为HCO3―的电离方程式,所以A错误;中和滴定时眼睛必须注意锥形瓶内溶液颜色的变化,故B正确,为本题的答案;电解水生成H2和O2的实验中,不必加入盐酸或硫酸增强导电性,若加入盐酸,则会生气氯气,故C错误;用等浓度(0.5 mol・L-1)等体积(50
?CO32―+H3O+为HCO3―的电离方程式,所以A错误;中和滴定时眼睛必须注意锥形瓶内溶液颜色的变化,故B正确,为本题的答案;电解水生成H2和O2的实验中,不必加入盐酸或硫酸增强导电性,若加入盐酸,则会生气氯气,故C错误;用等浓度(0.5 mol・L-1)等体积(50
本题难度:简单