ʱ��:2017-01-15 17:52:22
1�������� ��10�֣�Ag2O2����п���Ե�ص������������ʣ���ͨ�����з����Ʊ�����KOH��������AgNO3��Һ,����Ag2O���������ַ�Ӧ�¶�Ϊ80���߽���߽�һ����K2S2O8��Һ�����ӵ�����������У���Ӧ��ȫ���ˡ�ϴ�ӡ���ո���õ�������Ʒ����Ӧ����ʽΪ2AgNO3��4KOH��K2S2O8 Ag2O2����2KNO3��K2SO4��2H2O
Ag2O2����2KNO3��K2SO4��2H2O
�ش��������⣺
��1�������Ʊ������У�����ϴ���Ƿ���ȫ�ķ�����??????????????????????????????
??????????????????????????????????????????????????????????????????????????��
(2)��п���Ե�صĵ������ҺΪKOH��Һ����طŵ�ʱ������Ag2O2ת��ΪAg��������Znת��ΪK2Zn(OH)4��д���õ�ط�Ӧ����ʽ��
???????????????????????????????????????????��
(3)ȷ��ȡ�����Ʊ�����Ʒ����Ag2O2����Ag2O��2.558g����һ������������ȫ�ֽ�ΪAg ��O2���õ�224.0mLO2����״���£���������Ʒ��Ag2O2��������������������ȷ��С�������λ����
�ο��𰸣���1��ȡ�������һ��ϴ����Һ������1��2��Ba(NO3)2��
���������
�����������1��ȡ�������һ��ϴ����Һ������1��2��Ba(NO3)2��Һ���������ְ�ɫ���ǣ���ʾ��ϴ����ȫ��ȡ�������һ��ϴ����Һ������1��2�η�̪��Һ������Һ���Ժ�ɫ����ʾ��ϴ����ȫ����
��2��Ag2O2��2Zn��4KOH��2H2O��2K2Zn(OH)4��2Ag
��3��n(O2)��224mL/22.4L��mL��1��1000mL�� L��1��1.000��10��2 mol
����Ʒ��Ag2O2�����ʵ���Ϊx, Ag2O�����ʵ�����Ϊy����
248g��mol��1 �� x �� 232
�����Ѷȣ�һ��
2��ѡ���� ��֪:25 ��ʱ,Ksp[Mg(OH)2]=5.61��10-12,Ksp(MgF2)=7.42��10-11������˵����ȷ����(����)
A��25 ��ʱ,����Mg(OH)2��Һ�뱥��MgF2��Һ���,ǰ�ߵ�c(Mg2+)��
B��25 ��ʱ,��Mg(OH)2������Һ����������NH4Cl����,c(Mg2+)����
C��25 ��ʱ,Mg(OH)2������20 mL 0.01 mol��L-1��ˮ�е�Ksp����20 mL 0.01 mol��L-1 NH4Cl��Һ�е�KspС
D��25 ��ʱ,��Mg(OH)2������Һ����NaF��Һ��,Mg(OH)2������ת����ΪMgF2
�ο��𰸣�B
���������Mg(OH)2���ܶȻ�С,����������Mg2+Ũ��ҪСһЩ,A��;N���Խ��Mg(OH)2�������OH-,�Ӷ���ʹMg(OH)2�ĵ���ƽ�������ƶ�,c(Mg2+)����,B��ȷ��Ksp�����¶��й�,��C��;D��,����MgF2���ܶȻ���С,���Գ�����������ܵķ������,����������MgF2����,��ȷ��
�����Ѷȣ�һ��
3������� (1) t��ʱNa2SO4���ܽ����S g���䱥����Һ�ܶ�d g��cm-3�����ʵ���Ũ��Ϊc mol��L-1��������������Һ�У�����X g��ˮNa2SO4������Ygˮ��ָ�t�棬���ܻ��W gâ�����壬���й�ϵʽ��ȷ����????��????
A��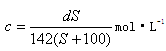
B��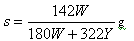
C��100X=YS
D��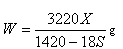
��2��������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
��֪��1molH��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ???????????��???????????��
�ο��𰸣�
��1��CD��2�֣�
��2��N2(g)��3H2(
���������
��A������ȷ�������λû�л��㣺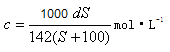 ��B������ȷ��
��B������ȷ��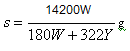 ��C D��ȷ��
��C D��ȷ��
�ơ�H=436kJ��3��946kJ�D3
�����Ѷȣ�һ��
4��ѡ���� ��֪п���仯����������������仯�������ơ���ͼ��������Ϊ��Һ��pH��������ΪZn2+���ӻ�[Zn(OH)4]2-���ӵ����ʵ���Ũ��(����Zn2+����Ũ��Ϊ10-5mol��L-1ʱ��Zn2+�����ѳ�����ȫ)������˵������ȷ����???? [???? ]
[???? ]
A����ZnCl2��Һ�м�������������������Һ����Ӧ�����ӷ���ʽ�ɱ�ʾΪ�� Zn2++4OH��=[Zn(OH)4]2��
B����ͼ�����ݼ���ɵ�Zn(OH)2���ܶȻ�Ksp=10-17 mol3��L-3
C��ij��Һ�к�Zn2+���ӣ�����Zn2+���ӿ��Կ�����ҺpH�ķ�Χ��8��12
D����1L1?mol��L-1 ZnCl2��Һ�м���NaOH������pH=7����NaOH?2mol
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ��2��10- 5mol/LKCl ��2��10- 5mol/LAgNO3��Һ�������ϣ�����˵����ȷ���� (��֪AgCl ��Ksp=1.8��10-10 )
A����AgCl��������
B����AgCl��������
C����ȷ������AgCl��������
D�����������AgCl
�ο��𰸣�B
���������
�����������2��10- 5mol/LKCl ��2��10- 5mol/LAgNO3��Һ�������ϣ���Һ�������Ӻ������ӵ�Ũ�ȷֱ���1��10- 5mol/L����ʱc(Ag��)��c(Cl��)��1��10-10��1.8��10-10 ������û�г�����������ѡB��
�����������ǻ���������Ŀ��飬Ҳ�Ǹ߿��е���Ҫ���㡣���������ǿ�����۽̲Ļ����������ڹ���ѧ���Ļ��������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷ�ܶȻ������ĺ��壬Ȼ��������������ü��ɡ�
�����Ѷȣ���