?
?????回答下列问题:
(3)上表所列实验中的“待测数据”指????????????????
(4)量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是
??????????????(填“酸式”或“碱式”)滴定管。
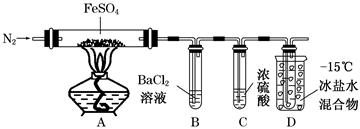
(5)若要证明实验Ⅱ中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住装置B中的乳胶管a,拔去干燥管上单孔橡皮塞,??????????????????????????????
(6)为探究CuO在实验Ⅱ中是否为催化剂,需补做如下实验(无需写出具体操作):
a.?????????????????????????????????,b.检验CuO的化学性质有没有改变。
参考答案:(1)①②③(2分)研钵(1分)
(2)向过滤器中的沉
本题解析:本题主要考查化学实验中一些基本操作,属中等难度。学生只要基本功扎实,(一)制取CuO的过程中主要考查了一些化学实验基本操作;(二)中实验时均以生成25 mL气体为准,故待测数据是收集到25ml气体时所需的时间,选用滴定管时,酸式滴定管下部有活塞,密封效果不如碱式滴定管,催化剂的定义中指出,催化剂在反应前后质量和性质均不改变,答案可得。
本题难度:一般
3、填空题 (16分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:

(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2 ==6SO2+Fe3O4,氧化产物为??????,若有3 mol FeS2参加反应, ==6SO2+Fe3O4,氧化产物为??????,若有3 mol FeS2参加反应,
转移???????mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为????????????。
(3)与明矾相似,硫酸铁也可用作净水剂,其原理为????????????(用离子方程表示)?
(4)①钢铁的电化腐蚀简单示意图如右,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。
②写出修改前的钢铁吸氧腐蚀石墨电极的电极反应式????????。
(5)铁红是一种红色颜料,其成分是Fe2O.3将一定量的铁红溶于160ml5 mol・L―1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为????。
参考答案:(1)SO2、Fe3O4???? 32?(2)2Fe3++C
本题解析:(1)根据方程式可知,FeS2中Fe和S的化合价分别从+2价升高到+8/3价和从-1价升高到+4价,所以FeS2是还原剂,SO2和四氧化三铁都是氧化产物;若有3 mol FeS2参加反应,转移电子的物质的量是(2+6×5)=32mol。
(2)铁离子具有氧化性,能氧化单质铜,方程式2Fe3++Cu=2Fe2++Cu2+。
(3)硫酸铁溶于水电离出的铁离子能水解生成氢氧化铁胶体,胶体具有吸附性,所以可作净水剂,方程式为Fe3++3H2O  本题难度:一般 本题难度:一般
4、选择题 有下列操作,对实验现象的描述,或由现象作出的判断错误的是( )
A.向溶解有Na2O2的水溶液中滴入2滴酚酞试液,溶液先变红振荡后褪色
B.向紫红色的酸性KMnO4溶液滴入足量的Na2SO3溶液,溶液紫红色褪去
C.向FeCl2溶液中滴入NaOH溶液,生成白色沉淀立即变灰绿色、最后变为红棕色
D.向某溶液中加入BaCl2溶液和稀HNO3,若有白色沉淀生成,则说明原溶液中含SO42-
参考答案:D
本题解析:
本题难度:一般
5、填空题 铁单质及其化合物在生活、生产中应用广泛。请回答:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应是???????????????。
(2)由于氧化性Fe3+>Cu2+氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是???????????????????????????????????????。
(3)硫酸铁可作絮凝剂,常用于净水,其原理是?????????????????(用离子方程式表示)。在使用时发现硫酸铁不能将酸性废水中的悬浮物沉降除去,其原因是??????????????????。
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4十4CO 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是????????????。 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是????????????。
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是??????(填字母)。
?
| 陈述Ⅰ
| 陈述Ⅱ
| 判断
| A
| 铁是地壳中含量最高的金属元素
| 铁是人类最早使用的金属材料
| Ⅰ对;Ⅱ对;有
| B
| 常温下铁与稀硫酸反应生成氢气
| 一定温度下氢气能还原氧化铁得到铁
| Ⅰ对;Ⅱ对;无
| C
| 铁属于过渡元素
| 铁和铁的某些化合物可用作催化剂
| Ⅰ错;Ⅱ对;无
| D
| 在空气中铁表面形成致密氧化膜
| 铁不能与氧气反应
| Ⅰ对;Ⅱ对;有
?
参考答案:(1)O2+2H2O+4e-=4OH-(2分)
(2)
本题解析:
试题分析:(1)在钢铁的吸氧腐蚀中,正极上发生的是氧气得电子的还原反应,即O2+2H2O+4e-=4OH-,
(2)三价铁的氧化性强于铜离子,所以金属铜可以和三价铁之间发生氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+,
(3)三价铁水解生成的氢氧化铁胶体具有净水作用,原理方程式为:Fe3++3H2O?Fe(OH)3+3H+,硫酸铁中由于三价铁水解导致溶液显酸性,而酸性环境中,氢离子抑制了铁离子的水解,无法生成氢氧化铁胶体,所以硫酸铁不能使酸性废水中的悬浮物沉降而除去,
(
本题难度:一般
|
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G
|