时间:2017-01-15 15:18:53
1、选择题 下列物质中含有化学键种类相同的是( )
A.NaF和H2O
B.D2O与TCl
C.Na2O与CO2
D.氢气与氦气
参考答案:A、NaF中只有离子键,H2O中只有共价键,所以化学键类型不
本题解析:
本题难度:简单
2、选择题 下列每组物质发生变化所克服的粒子间的作用不属于同种类型的是
A.金刚石和金属钠熔化
B.碘和干冰受热升华
C.氯化钠和氯化钙熔化
D.氯化氢和溴化氢溶于水
参考答案:A
本题解析:
试题分析:A、金刚石和金属钠形成的晶体分别是原子晶体和金属晶体,熔化克服的作用力分别是共价键和金属键,A正确;B、碘和干冰形成的晶体均是分子晶体,升华克服的是分子间作用力,B不正确;C、氯化钠和氯化钙形成的晶体均是离子晶体,熔化克服的是离子键,C不正确;D、氯化氢和溴化氢溶于水均电离出离子,克服的是共价键,D不正确,答案选A。
本题难度:一般
3、选择题 下列物质中,既含有离子键,又含有非极性共价键的是(???)
A.Na2O2
B.NaOH
C.CaCl2
D.H2O2
参考答案:A
本题解析:
试题分析:Na2O2中既含有离子键,又含有非极性共价键,故A正确,为本题的答案;NaOH含有离子键和极性共价键,故B错误;CaCl2中只含有离子键,故C错误;H2O2中不含有离子键,故D错误。
本题难度:一般
4、选择题 下列叙述中正确的是(??)
A.极性分子中不可能含有非极性键
B.离子化合物中不可能含有非极性键
C.非极性分子中不可能含有极性键
D.共价化合物中不可能含有离子键
参考答案:D
本题解析:
试题分析:A、H2O2是极性分子,含有非极性键,故错;B、Na2O2是离子化合物,含有非极性键,故错;C、CO2是非极性分子,含有极性键,故错。故选D。
点评:本题考查的是化学键和分子的极性的相关知识,题目难度不大,熟悉各个用语的含义是解题的关键。
本题难度:简单
5、选择题 下列用电子式表示化合物的形成过程正确的是(???)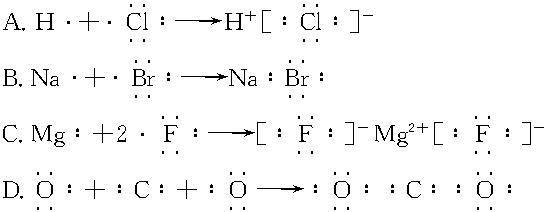
参考答案:C
本题解析:A项中生成的HCl是共价化合物;B项中生成的NaBr是离子化合物;D项中电子数有误。
本题难度:简单