时间:2017-01-15 15:18:53
1、选择题 下列叙述正确的是
A.糖尿病人应少吃含糖的食品,某八宝粥中注明未加糖,糖尿病人可以放心食用
B.反应2NO2(g)→N2O4(l)的熵(体系混乱度)减小(即ΔS<0)
C.环境保护的根本是研究怎样将污染物质转化为有用物质
D.ΔH>0的化学反应一定不能自发进行
2、选择题 氯的含氧酸根离子有ClO-、ClO2-、ClO3-、ClO4-等,有关它们的下列说法正确的是
A.ClO-中氯元素显+1价,具有很强还原性
B.这些离子结合H+的能力,ClO4-最强
C.这些离子中的氯原子都采取sp3杂化
D.ClO3-是NO3-的等电子体,其空间构型为平面三角形
3、选择题 同学对“CO2是共价化合物和NH4Cl是离子化合物”有下列四点感悟,其中不正确的是
A.离子化合物中可能含共价键
B.共价化合物中一定不含离子键
C.离子化合物中不一定含金属元素
D.离子化合物中一定不含共价键
4、实验题 (18分)50 mL0.5mol/L盐酸跟50mL0.55mol/L氢氧化钠溶液在下图装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题。
(1)实验目的:
(2)实验用品:烧杯(500 mL和100 mL各1只)、温度计、塑料泡沫板(或硬纸板)、泡沫塑料或纸条、 (填写所缺的实验仪器);0.50mol/L盐酸、0.55mol/L NaOH溶液
(3)实验步骤:(略)
(4)问题与结论:
①完整地做一次这样的实验,需测定 次温度。
②大小烧杯间填满碎纸条、大烧杯上加盖硬纸板的作用是 。
③该实验中NaOH溶液的浓度大于盐酸浓度的作用是 。
④大烧杯上如不盖硬纸板,对求得中和热的数值有何影响: 理由:
⑤改用60 mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液进行反应,与上述实验相比,所放热量是否相等: 所求中和热数值是否相等: 。
5、填空题 研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气。下图表示恒压容器中0.5 mol CO2和1.5 mol H2转化率达80%时的能量变化示意图。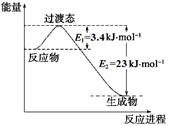
①写出该反应的热化学方程式: 。
②能判断该反应达到化学平衡状态的依据是 。
a.容器中压强不变 b.H2的体积分数不变
c.c(H2)=3c(CH3OH) d.容器中密度不变
e.2个C=O断裂的同时有6个H-H断裂。
(2)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH原理的示意图。根据要求回答问题: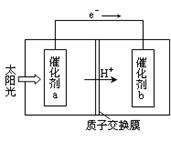
①该过程是将 转化为 。(以上两空选填“电能”“太阳能”“化学能”)
②催化剂b表面的电极反应方程式为 。
(3)某国科研人员提出了使用氢气和汽油(汽油化学式用C8H18表示)混合燃料的方案,以解决汽车CO2的排放问题。该方案主要利用储氢材料CaH2产生H2和用汽油箱贮存汽油供发动机使用,储氢系统又捕集汽油燃烧产生的CO2,该系统反应如下图所示: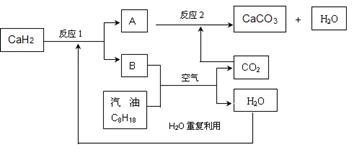
解决如下问题:
①写出CaH2的电子式 。
②反应1中氧化剂与还原剂的物质的量之比是: 。
③如该系统反应均进行完全,试写出该系统总反应的化学方程式 。