时间:2017-01-13 09:39:31
1、填空题 Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表: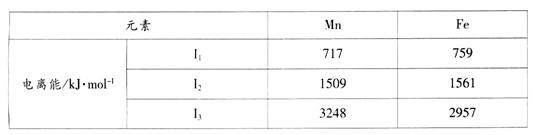
回答下列问题:
(1)Mn元素价电子的电子排布式为???????????????????????,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fen再失去一个电子难。其原因是???????????????。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是????????????。
②络离子[Fe(CN)6]4-的配体CN-中C原子的杂化轨道类型是???????????,写出一种与 CN-互为等电子体的单质分子的电子式??????????????????????????。
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体类型为????????????????。
(4)金属铁晶体在不同的温度下有两种堆积方式,如图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为?????????????。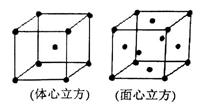
2、填空题 【物质结构与性质】
碳元素可以组成不同的单质和化合物。
(1)碳原子的电子排布来源:91考试网 www.91exAm.org图为_______________
(2)由C和同周期的元素组成的分子如图a,推测分子式是____________,键角为_______。 图a
图a
(3)CO2分子的结构式为__________,与它等电子体的分子有___________;
(4)第ⅡA金属碳酸盐分解温度如下:
| ? | BeCO3 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 分解温度 | 100℃ | 540℃ | 960℃ | 1289℃ | 1360℃ 碳酸盐中CO碳原子是________杂化,其空间构型为________________。 解释上列碳酸盐分解温度越来越高的原因是_________________________。 (5)锂电池负极材料晶体为Li+嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图2 晶胞结构,化学式为____________________。Li+投影在石墨层图,试在图中标出与该离子邻近的其它六个Li+的投影位置。 在晶胞中,给出的平行六面体的棱长单位为nm,相对原子质量Li:7、C:12。 则锂电池负极材料的密度为_____________g・cm-3(用含a、b代数式表示)。 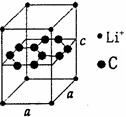 ??? ???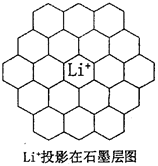 图2?????????????????????????图3 3、填空题 2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、lnGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。 4、选择题 石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如图所示),可由石墨剥离而成,具有极好的应用前景。下列说法正确的是 5、填空题 过氧化氢(H2O2)的水溶液俗称双氧水,其水溶液可用于制备工业上的漂白剂、特殊环境里燃料燃烧的助燃剂、医疗上的消毒剂、实验室里的制氧剂;过氧化钠(Na2O2)可用于制备工业上的漂白剂、特殊环境里的供氧剂、实验室里的制氧剂。过氧原子团“O2”由2个氧原子共用1对电子组成。 ?? |