时间:2017-01-13 09:34:14
1、选择题 下列关于实验现象的描述不正确的是????????(???)
A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B.葡萄糖与新制的氢氧化铜悬浊液混合,加热,有红色沉淀生成
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
参考答案:C
本题解析:略
本题难度:一般
2、选择题 把铁片放入下列溶液中,铁片溶解且固体的总质量减小,并伴有气体产生,则该溶液是(???)
A.稀硫酸
B.CuSO4
C.Na2SO4
D.浓硫酸
参考答案:A
本题解析:
试题分析:铁和稀硫酸反应生成硫酸亚铁和氢气,符合题意;铁和硫酸铜反应生成氯化亚铁和铜,该题质量增加;铁和硫酸钠不反应,在浓硫酸中发生钝化,均不符合题意,答案选A。
点评:该题是基础性试题的考查,侧重对学生基础性知识的巩固和训练,有利于培养学生灵活运用基础知识解决实际问题的能力,该题是识记性知识的考查,难度不大,记住即可得出结论。
本题难度:简单
3、实验题 (15分)Fe2O3俗称氧化铁红,常用作油漆着色剂。工业以煤矸石(主要成分:SiO2 49.5%;Fe2O3 20.6%;Al2O318.9%,以及MgO、FeO等其他杂质)制备并研究氧化铁红的应用。
(一)制备氧化铁红
1.预处理:将煤矸石粉碎,在350℃下焙烧2小时。
2.加酸溶解:将预处理后的煤矸石溶于质量分数为15%过量的硫酸溶液中,过滤。在滤液中加入的H2O2。
3.调节pH:在上述滤液中加1mol/LNaOH溶液调节溶液的pH,再过滤,得到滤渣。
4.产品处理:将滤渣进行水洗、烘干、煅烧、研磨、过筛得产品。
已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 1.3 | 3.3 | 7.5 | 10.3 |
| 完全沉淀 | 2.8 | 5.2 | 9.7 | 12.2 请回答下列问题: (1)预处理时,将煤矸石焙烧2小时的目的是??????????????????????。 (2)酸浸操作中,过量H2SO4的作用是??????????????????????????。 在实验室中进行该操作时,用到玻璃仪器有??????、?????。 (3)用NaOH溶液调节pH的最佳范围是??????。若从第二次过滤的滤液中获取较纯净的硫酸镁晶体,应补充的操作是??????????????????????????、洗涤后,干燥即得。 (4)产品处理时,对滤渣水洗的操作是 ????????????????????????。 (二)分析与讨论: 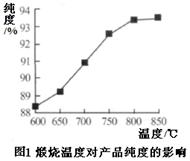 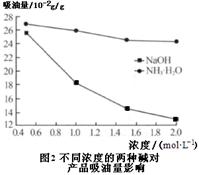 (5)产品处理时,煅烧温度对产品的纯度有很大影响。已知温度对产物纯度的影响如图1所示,则煅烧时温度最好控制在?????℃。 (6)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图2所示,则上述生产中在调节溶液pH时,选用NaOH溶液而不选用氨水的原因是???????????????????????。 参考答案:(1)将煤矸石中的矿物转化为氧化物,便于酸浸????(2分) 本题解析: 本题难度:一般 4、选择题 将Cu片放入0.l mol / L FeCl3溶液中,一定时间后取出Cu片,溶液中c(Fe3+)∶c(Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为 参考答案:D 本题解析:设参加反应的铜的物质的量是x,则根据方程式Cu+2Fe3+=Cu2++2Fe2+可知,消耗铁离子是2x,生成亚铁离子是2x,则溶液中铁离子的物质的量是2/3×2x=4x/3,所以溶液中铜离子和铁离子的物质的量之比是3 : 4,答案选D。 本题难度:简单 5、选择题 将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是(? ) 参考答案:C 本题解析:n(Fe)= 本题难度:一般 |